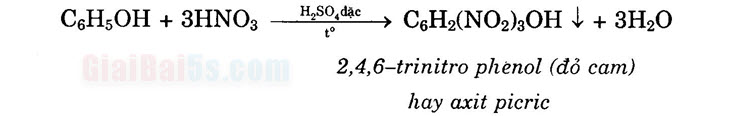| A. KIẾN THỨC CẦN NHỚ
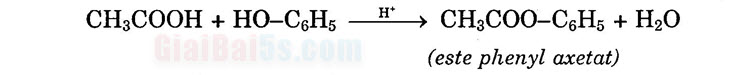
Tính chất hóa học. 1) Tính chất của nhóm –OH gây ra: a) Phản ứng với kim loại kiềm: 2C6H5OH + 2Na → 2C6H5ONa+ H2↑ 2CH3-C6H5-OH + 2Na → 2CH3-C6H4-ONa + H2↑ b) Tác dụng với dung dịch kiêm: C6H5OH (khó tan) + NaOH → C6H5ONa (dễ tan) + H2O Chú ý: Phản ứng tái tạo phenol từ natri phenolat. C6H5ONa + CO2 + H2O → C6H6OH + NaHCO3 c) Phản ứng este (rất khó):
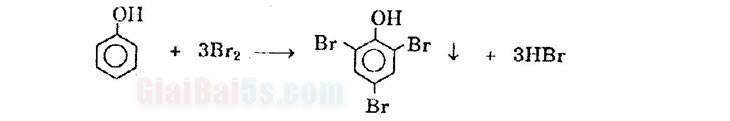
Chú ý: Để điều chế este phenylaxetat, ta cho phenol tác dụng với anhidrit. (CH3CO)2O + C6H5OH → CH3COOC6H5 + CH3COOH Phenol không tham gia phản ứng thế nhóm –OH khi tác dụng với axit HCl, HBr, H2SO4… 2) Tính chất do nhân benzen gây nên: a) Tác dụng với brom:
b) Tác dụng với HNO3 / H2SO4 đặc (phản ứng nitro hóa).
c) Phản ứng với H2:
|


Nguồn website giaibai5s.com
- HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 232 – 233 Câu 1. – Câu đúng: b;
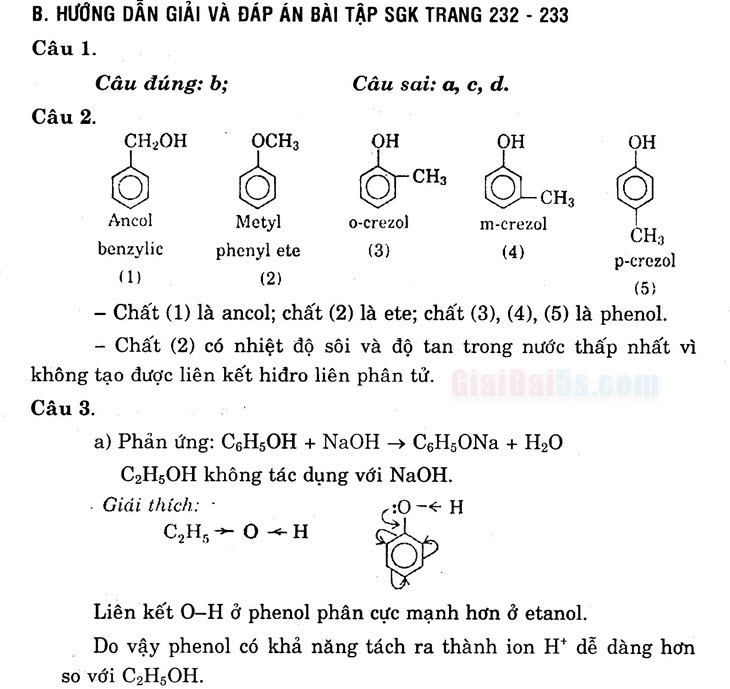
Câu sai: a, c, d. Câu 2. CH,OH . OCH OH OH
© OCH OCHO Ancol Metyl 0-crezol
ezol m-crezol CH, benzylic phenyl ete (3)
p-crezol (1) (2)
(5) – Chất (1) là ancol; chất (2) là ete; chất (3), (4), (5) là phenol.
– Chất (2) có nhiệt độ sôi và độ tan trong nước thấp nhất vì không tạo được liên kết hiđro liên phân tử. Câu 3.
- a) Phản ứng: C6H5OH + NaOH + C6H5ONa + H2O | C2H5OH không tác dụng với NaOH. Giải thích:
:0-H C,H, + 0 +H
OH
OH
Liên kết 0–H ở phenol phân cực mạnh hơn ở etanol. .
Do vậy phenol có khả năng tách ra thành ion H+ dễ dàng hơn so với C2H5OH.
1
. b)
Do các hiệu ứng trên mà mật độ electron ở vòng benzen của phenol cao hơn mật độ electron ở vòng benzen của nitrobenzen. Phản ứng thế vào vòng benzen do các tiểu phân tích điện dương tấn công. Do vậy mật độ electron cao hơn thì phản ứng thế dễ hơn. Câu 4.
OH . . . OH
M
0
+ 3H,
gumpar
O
| Tách dựa vào tính chất vật lí và hóa học:
Hòa tan hỗn hợp hai chất nào dung dịch NaOH đặc để chuyển C6H5OH thành C6H5ONa tan trong nước. Xiclohexanol tan trong nước nên được chiết khỏi dd C6H5ONa. Trong dung dịch còn C6H5ONa, đem thực hiện phản ứng để hoàn nguyên phenol.
C&H:ONa+ CO2 + H2O → C6H5OH+ + NaHCO3 Câu 5.
–
a)
.
.
он
OH
C2H5OH
Nước brom | Kết tủa trắng | Tan hoàn toàn
Tan ít, phân thành lớp nổi lên trên
CH2-OH
CHCI
CH – OH
CH3
Không hiện tượng
CH-OH Dung dịch xanh trong suốt
Không hiện tượng
Cu(OH)2
AgNO3
- Agcit
Câu 6. Phản ứng:
OH
Br.
-Br + 3HBr (1)
+ 3Br
0,04 mol 0.gamot. B
0,04
4 mol 0,04mol
Br
0,04moi
TNM
CH=CH2 C HBr-CH_Br O + Br2 = 0 0,02mol 0,02mol
HBr + NaOH + NaBr + H2O
(3)
(mol) 0,04
0,04
www
Số mol NaOH tham gia phản ứng (3) là:
.
1,11 x 14,4 x 10
~0,04 (mol) 100 x 40
Số mol Bry tham gia phản ứng (1) và (2) là:
300 x 3,2 – 0,06 (mol)
100 x 160
Đưa số liệu lần lượt vào các phương trình phản ứng để tính ta có kết quả:
mphenol = 94 * 0,04 – 1,253 (gam)
3
1253
→ %m4,01 = 1,253 + 2,08
* 100% = 37,59%.
.
.
Và mstiren = 104 x 0,02 = 2,08 (gam)
B%m, H. CHÚCH, = 100% – 37,59% = 62,41%