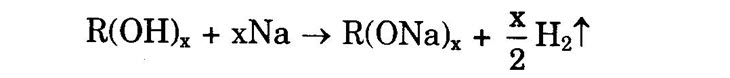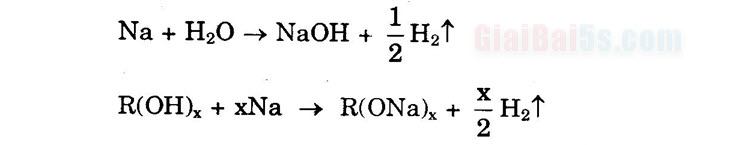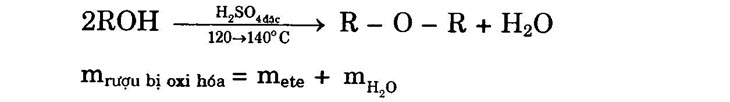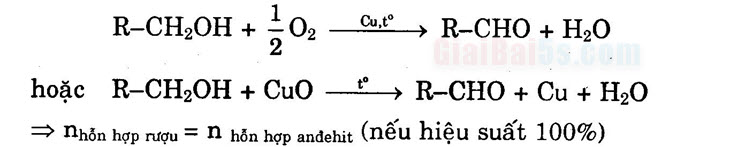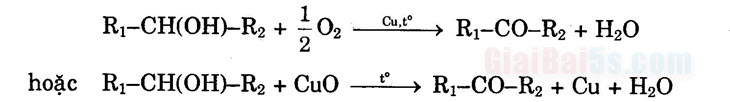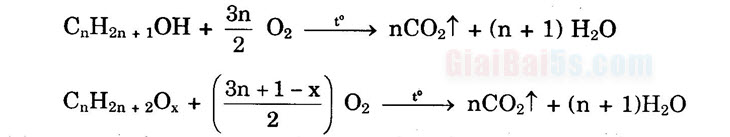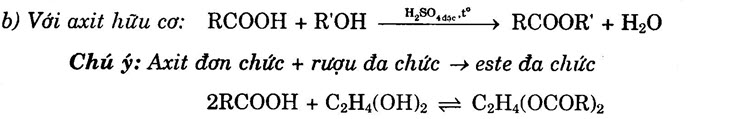| A. KIẾN THỨC CẦN NHỚ
Tính chất hóa học 1) Tác dụng với kim loại kiềm(Na, K): Từ số mol Hy sinh ra, suy ra số nhóm –OH). Chú ý: – Khi dung dịch rượu (dung môi H2O) tác dụng với kim loại kiềm thì có 2 phản ứng:
– Trong trường hợp này, thể tích H2 có cả H2O tạo nên. Nếu rượu trong benzen hoặc hexan thì chỉ có rượu phản ứng với Na. – Phản ứng tái tạo rượu: RONa + H2O → ROH + NaOH: chứng tỏ rượu không phải là axit. 2) Phản ứng tách nước từ rượu (đề hiđrat hóa): a) Loại một phân tử nước từ 1 phân tử rượu (tạo anken):
b) Loại 1 phân tử H2O từ 2 phân tử rượu (tạo ete):
3) Phản ứng oxi hóa không hoàn toàn rượu: a) Rượu bậc 1 khi oxi hóa cho anđehit:
b) Rượu bậc II oxi hóa hoàn toàn thành xeton:
c) Rượu bậc III khó bị oxi hóa:
Khi oxi hóa không hoàn toàn rượu bậc I có thể thu được axit, anđehit tương ứng (cùng số C), rượu dư và nước. Hóa tính của sản phẩm này rất phức tạp, cần xét cụ thể từng trường hợp. 4) Phản ứng oxi hóa hoàn toàn (đốt cháy)
Chú ý: Nếu sản phẩm cháy có nụ.0 > no, thì rượu đem đốt là rượu no. mO/rượu + mO/kk = mO/CO2 + mO/H2O 5) Phản ứng với axit: a) Axit vô cơ:
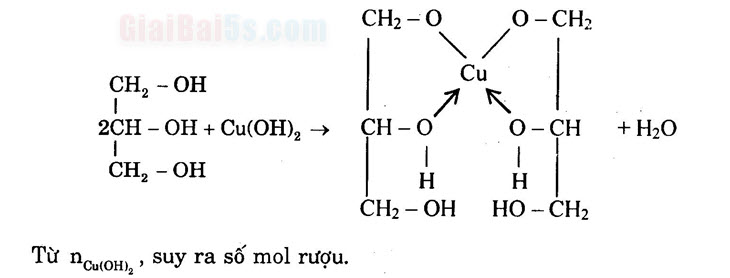
Chú ý: Nếu R trong rượu không no thì sẽ kèm theo phản ứng cộng vào gốc R. 6) Phản ứng với Cu(OH)2 Chỉ có rượu đa chức có các nhóm (-OH) đính vào các nguyên tử cacbon kế tiếp nhau cho phản ứng hòa tan Cu(OH)2 tạo thành dung dịch màu xanh lam:
|




Nguồn website giaibai5s.com
- HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 224 – 228 – 229
. 1. Định nghĩa, phân loại, đồng phân, danh pháp và tính chất vật lí Câu 1. (a): D; (b): H. Câu 2.
Gọi tên: a) CH3CH2CH2CH2OH: ancol butylicl (butan-1-ol) (bậc I) b) CH3CH(OH)CH2CH3: ancol sec-butylic (butan-2-ol) (bậc II) c) (CH3)3COH: ancol tert-butylic (2-metylpropan-2-on) (bậc III) d) (CH3)2CHCH3CH2OH: ancol iso-amylic (3-metylbutan-1-on) (bậc I) e) CH = CH – CH2OH: ancol anlylic (propp-2-en-1-ol) (bậc I) g) CH,OH : ancol benzylic (phenylmetanol) (bậc I)
Câu 3.
Viết công thức: a) (CH3)2CHCH2OH’. b) (CH3)2CHCH,CH,OH c) CH3CH2CH2CH(OH)CH(CH3)2
- d) A
DI:
VOH
- e) CH2 = CHCH2CH2OH.
- g) C&H:CHCH,OH | Câu 4.
Ta có: neo, 394 = 0,06 (mol) và ngo 1,62 = 0, 09 (mol)
mc = 0,06 x 12 = 0,72 (gam); mio = 0,09 2 = 0,18 (gam)
mo = 1,38 – (0,72 +0,18) = 0,48 (gam); mß = 23 x 2 = 46 (gam) Gọi CTPT A là C,H,O, (x, y, z: nguyên dương)
12x:y: 162 = 0,72 : 0,18 : 0,48 = x:y: z = 2:6:1 Công thức đơn giản: C2H6O + (C2H6O)n = 46 | Vậy A: C2H5OH và B: CH3–0–CH3.
Câu 5.
CH3CH2CH2CH2CH2OH: ancol pentylic (ancol amylic); pentan-1-ol CH3CH2CH2CH(OH)CH3: pentan-2-ol CH3CH2CH(OH)CH2CH3: pentan-3-ol (CH3)2CHCH2CH2OH: ancol isoamylic; 3-metylbutan-1-ol (CH3)2C(OH)CH,CHz: ancol tert-pentylic; 2-metylbutan-2-ol CH(OH)CH(CH3)CH2CH3: 2-metylbutan-1-o!
(CH3)3CCH,OH: ancol neopentylic; 2,2-dimetylpropan-1-ol. Câu 6.
- a) CH3OH có nhiệt độ sôi cao hơn, tan tốt trong nước hơn CH3OCH3. b) C2H5OH có nhiệt độ sôi cao hơn, tan tốt trong nước hơn C2H5OCH.
- c) CHF (t°s = -38°C); C2H5OH (ts = 78,3°C). CH3OH có nhiệt độ sôi cao hơn, tan tốt trong nước hơn C2H5F.
- d) C6H5CH2OH có nhiệt độ sôi cao hơn, tan tốt trong nước hơn C&H OCHZ.
+) Giải thích: Rượu tạo được liên kết hiđro liên phân tử còn ete và C2H5F không tạo được liên kết hiđro liên phân tử.
- Tính chất hóa học, điều chế và ứng dụng Câu 1. Đáp án: C. Câu 2. a) 2CH2CH(OH)CH2 _HySOddəc, 140°C » (CH3),CHOCH(CH3)2 + H20
đisopropylete b) 2CH2OH + H2SO4đặc → (CH3)2SO4 + 2H,0
đimetyl sunfat c) CH CH(OH)CH2 + HBr _HySOddics t°C , CH,CHBrCH2 + H2O
2-brom propan d) (CH),CHCH,CH,OH _H2SO4dăc, t°C, (CH),CHCH=CH, + H2O ancol isoamylic
3-metylbut-1-en Câu 3.
CH2CH=CH2 + Cl, -_450°C, CH,CICH=CH2 + HCI CH,CICH=CH2 + Cl2 + H2O → CH CICH(OH)CH2Cl + HCI CH,CICH(OH)CH2Cl + 2NaOH → CH (OH)CH(OH)CH,OH
+ 2NaCl
1
112n + 1
Câu 4. Theo phương pháp ghép ẩn số: . Gọi hai đồng đẳng kế tiếp: CnH2n +1ONa và CmH2m + 1; m = n + 1
CnH2n+ OH + Na -> CH2n + ONa + H2 (mol) x
CyH2m + 2OH + Na → C„H2M + 2ONa + H, *(mol) y Lập hệ phương trình: (14n +18)x + (14n + 32)y = 16,6
0,5x
3
U m112M + 1
m
12m
+
1
0,5y
(x + y = 0,3
y = 0,8 – 0,3n Biện luận: y > 0 = 0,8 – 0,3n > 0 = n < 2,67 y < 0,3 – 0,8 – 0,3n < 0,3 = n > 1,7 = C2H5OH và C3H-OH. Tính % khối lượng: 46x + 60y = 16,6
x + y = 0,3 Giải hệ phương trình: x = 0,1 hay 4,6 gam C2H5OH, y = 0,2 hay 12 gam C3H,OH Vậy : %me, H, H = x 100% = 27,71%
%mc,H,OH = 16,6%
12 2_*100% = 72, 29%
askt
Câu 5. a) +) Sơ đồ học sinh đề nghị điều chế CH3OH:
CHA _Cly, as → CH,Ci_H30, OH CH3OH CH4 + Cl2 _askt — CH2Cl + HCI
CH, CI + NaOHť → CH3OH + NaCl +) Theo sơ đồ trên thì:
– Lãng phí giai đoạn tạo ra CH3Cl về hóa chất và thời gian.
– Thải HCl độc hại vào môi trường. Ngoài ra (CH4 + Cl2) tạo ra hỗn hợp các dẫn xuất thế nên sản phẩm kém tinh khiết. +) Sơ đồ học sinh đề nghị điều chế C2H5OH:
CH2=CH2 + H2 _Ni → CH3-CH3 CH3-CH3 + Cl2 __ askt → CH3CH2Cl + HCI CH3-CH2Cl + NaOH CH3-CH,OH + NaCl
Sơ đồ này bất hợp lí ở chỗ biến etilen là một chất có khả năng phản ứng cao hơn, chọn lọc hơn thành etan là một chất có khả năng phản ứng thấp, kém chọn lọc hơn, do đó tiêu tốn các hóa chất đắt tiền như Cl2, NaOH, Hg, nhiều giai đoạn, thải HCl độc hại vào môi trường giai đoạn clo hóa hình thành hỗn hợp sản phẩm khó tách biệt. b) Sơ đồ áp dụng trong công nghiệp:
2CH4 + 02 – 200°C, 100atın, Cu → 2CH3OH . . .. .
CH2=CH2 + H20 – tee . HșPO• → CH2CH2OH
- CH., Cả hai sơ đồ chỉ gồm một giai đoạn, sử dụng hóa chất rẻ tiền (O2, H2O) không thải khí độc. Câu 6.
- a) – Lấy ở ống nghiệm mẫu ra mỗi lần ít để thử được nhiều lần.
– Lần lượt cho từng chất (1), (2), (3) tác dụng với Cu(OH)2 thì nhận ra chất (3) với dấu hiệu tạo ra phức chất màu xanh trong suốt.
– Lần lượt cho từng chất (1), (2) tác dụng với Na thì nhận ra chất (2) với dấu hiệu khí H2 bay ra.
– Còn lại là chất (1). b) Xiclopentanol (1); pent-4-en-1-ol (2); gliserol (3)
– Lần lượt cho từng chất (1), (2), (3) tác dụng với Cu(OH)2 thì nhận ra glixerol
– Thử 2 chất còn lại với dung dịch brom, chất nào làm mất màu dung dịch brom nhận được pent-4-en-1-ol.
– Còn lại là xiclopentanol . . | Câu 7. a) CH,
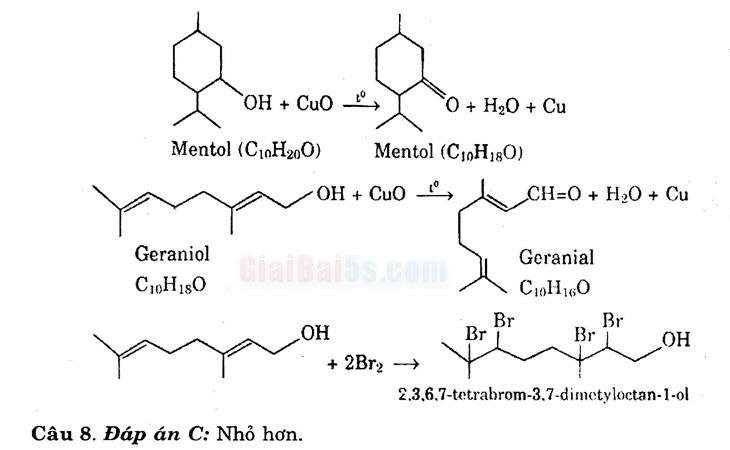
Mentol là ancol no bậc 2. CH, CH,
Tên theo IUPAC là: CH., CH-OH
5-metyl-2-isopropylxiclohexan-1-ol.
.
.
CH
C.-H CH, CH, HọG CH
GH, ACH
OH Geraniol là ancol không no
bậc 1 theo IUPAC là: 3,7-dimetyl octa-2,6-dien-1-ol..
CH;
CH:
Y OH + CuO Y O + H2O + Cu Mentol (C10H200) Mentol (C19H180)
A OH + Cuo , LCH=O + H20 + Cu
Geraniol CloH180
Geranial
C10H160 . OH
Br Br
Bra BrOH . + 2Br27
2.3,6,7-tetrabrom-3,7-dimetyloctan-1-01
M
+2Br,
w
!
–
–
–
MALI TA’
| Câu 8. Đáp án C: Nhỏ hơn.