

Nguồn website giaibai5s.com
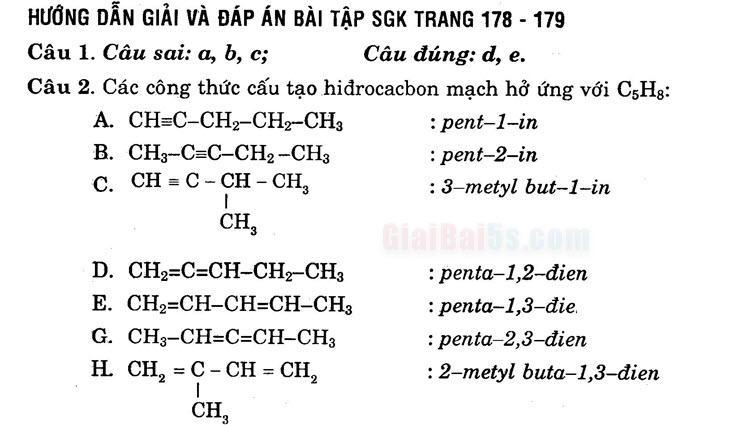
HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 178 179 Câu 1. Câu sai: a, b, c Câu đúng: d, e. Câu 2. Các công thức cấu tạo hidrocacbon mạch hở ứng với C3Hg:
- CH=C-CH2-CH2-CH3 : pent-1-in B. CH3-C=C-CH2-CHg : pent-2-in C. CH = C – CH – CH,
: 3-metyl but-1-in CH
- CH2=C=CH-CH2-CH3 E. CH2=CH-CH=CH-CH2 G. CH3-CH=C=CH-CH3 H. CH = C – CH = CH,
:penta-1,2-đien : penta-1,3-đien : penta-1,3-đien 12-metyl buta-1,3-đien
..
CH,
: 3-metylbuta-1,2-dien
- CH, -C = C = CH..
, CH, . .
–
- CH2=CH-CH2-CH=CH2 : penta-1,3-dien (A), (B) đồng phân vị trí liên kết ba. (A) và (C), (B) và (C) là đồng phân mạch cacbon. (D), (E, (F), (G) cũng như (H), (I) là đồng vị trí liên kết đôi. (D), (E), (G), (F) là đồng phân mạch cacbon với (H) và (I).
(A), (B), (C) và (D), (E), (F), (G), (H), (I) là đồng phân nhóm chức. Câu 3.
| Các phản ứng:
- a) CH3-CECH + 2H, -_ Ni → CH3-CH2-CH3 b) CH3-C=CH + H,
H._ Pd CH3-CH=CH2
2 PbCO. CH3-CH=CH2 c) CH3-C=CH + Br2 — CCI → CH3-CBr=CHBr
-20°C d) CH3-C=CH + 2Br2 Solec → CH3-CBrz-CHBr, e) CH3-C=CH + [Ag(NH3)2]OH → CH2C=CAg+ + 2NH3 + H20 g) CH3-C=CH + 2HCl (k) + CH3-CC12-CH3
- h) CH3-C=CH + H2O → CH3-CO-CH3 Câu 4.
- a) Dùng dung dịch AgNOM/NH nhận ra CH2: có kết tủa màu vàng nhạt. Dùng dung dịch nước brom nhận ra C2H4: làm mất màu dung dịch Br2, còn lại là etan.
- b) Dùng dung dịch AgNO/NH nhận ra but-1-in có kết tủa vàng nhạt còn lại là butađien.
- c) Dùng dung dịch AgNO/NH nhận ra but-1-in có kết tủa vàng nhạt còn lại là but-2in. Câu 5.
- a) Phương pháp đi từ CH được dùng nhiều vì CH có nhiều trong khí thiên nhiên và sản phẩm chế biến dầu mỏ, còn phương pháp đi từ đá vôi tốn năng lượng nhiều hơn cho khí axetilen có lẫn nhiều tạp khí (H2S, NH3, PHg) là những khí độc có hại, giá thành cao hơn. b) CH=CH +HCI
on → CH2=CHCI HgCl2, 150°C-200°C CH=CH, Boobce → CH=CHCI
- c) Phương pháp đi từ etilen cho sản phẩm rẻ hơn vì CH2=CH2 có sẵn trong khí cracking còn CH=CH phải điều chế từ CH ở 1500°C tốn năng lượng, đắt hơn. (xem phần từ liệu bài 42 SGK tr. 164). Câu 6.
Phương trình phản ứng: 20H – 1500°C) CH=CH + 3H2 (1)
CH=CH + 2[ Ag(NH3)2]OH → Ag-C=C-Ag + 2H20 + 4NH3 (2)
- a) Theo phương trình phản ứng (1) nếu gọi số mol C2Hg sinh ra • là x thì số mol hỗn hợp khí sau phản ứng nhiệt phân là:
3,36 + 2x = 0,15 + 2x
22.4 Theo đầu bài thể tích hỗn hợp giảm 20% là thể tích CHỊ:
- 100%
2x + 0.15 = 20%
Tính được x = 0,05 (mol) Nếu phản ứng đạt hiệu suất 100% thì số mol C2H, là 9,15 (mol) Vậy hiệu suất phản ứng nhiệt phân là: 0,05 x 100% = 66, 67%
0,075 b) % VCH, = 20%; VH, = 60%; % VCH, = 20%.
- c) Cho hỗn hợp qua dung dịch AgNO/ NH3 dư, thu lấy dung dịch rồi cho phản ứng với dung dịch H2SO4 loãng, dư thu được C2Hg.
