



Nguồn website giaibai5s.com
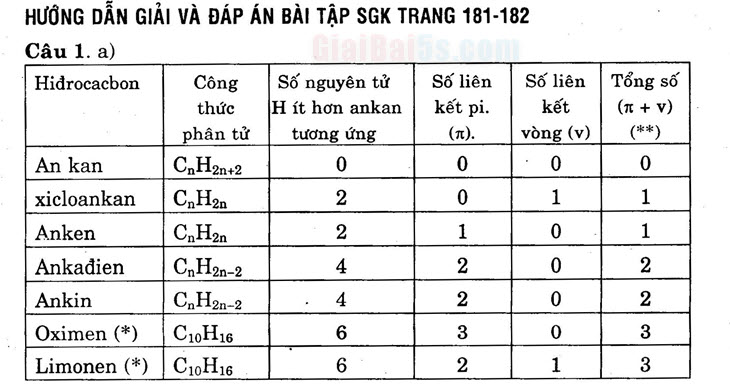
HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 181-182 Câu 1. a) Hiđrocacbon Công | Số nguyên tử Số liên Số liên Tổng số
| thức H ít hơn ankan | kết pi. kết (10 + v) phân tử 1 tương ứng
(at).
vòng (v) (**) An kan xicloankan | CnH2n Anken CnH2n Ankađien CnH2n-2 Ankin
CnH2n-2 Oximen (*) C10H16 Limonen (*) C10H16
(*) Công thức cấu tạo cho ở bài “Khái niệm về tecpen”. B. (**) dùng kí hiệu ( + v) trong các bài tập sẽ có lợi và gọn. .
- b) Số nguyên tử H ở xicloankan ít hơn ankan 2 nguyên tử vì xicloankan có 1 vòng no. Anken có số nguyên tử H ít hơn ankan vì anken có 1 liên kết T. Ankin, ankađien có số nguyên tử H ít hơn ankan 4 nguyên tử vì chúng có hai liên kết T. . Câu 2. .. ..
- a) (1), (2): C; (3): E; (4): K; b). (5): G; (6): A; (7): H; (8): K. Câu 3. a) Menton có CTPT C4H8O có: 1 + y = 2*10+2 -18_0
P = 2(m + y = 2; T = 1 và v = 1) .
2 x 20 + 2 – 30 | b) CTPT của vitamin A là CaoHaoO có: 1 + y =
. 2 (T + y = 6; v = 18 T = 5, không có liên kết ba, vậy số liên kết đôi
là 5). Câu 4. a) Anken Ankađien
Ankin CTTQ
RiR3
Ri
Rz
‘c-c
C=
.
RS
R? -C=C – R
RA
R4
Ral
:
:
Rol
,
Đặc điểm | 2 nguyên tử C mang | 4 nguyên tử C của | 2 nguyên tử C Cấu trúc nối đôi ở trạng thái | buta-1,3-đien đều ở 1 liên kết ba ở không
| sp43. 2 nguyên tử C | trạng thái sp=?, cả | trạng thái lai gian và 4H nằm cùng 10 nguyên tử nằm hóa sp (lai hóa
trên mặt mặt | trên một mặt nằm trên phẳng. phẳng.
đường thẳng). b) Nhóm nguyên tử C=C-C=C và C=C quyết định tính chất hóa | học của anken, ankađien, ankin vì chúng có liên kết T kém bền.
- c) Những phản ứng đặc trưng của anken, ankađien và ankin là: . +) Phản ứng cộng: – Hạ, xt: Ni, Pt, hoặc PdPbCO3
– Halogen – HA. +) Phản ứng trùng hợp. +) Phản ứng oxi hóa: dd KMnO4..
:
n+2
AL
Câu 5.
- a) Nguyên tắc chung để điều chế anken, ankađien, ankin và tách hiđro ra khỏi ankan. Ví dụ: CnH2n+2 – to, xt → CH3 + H2
CaHa to, xt → C2H4 + H2
C.H2n+2_to,xt → CH2n-2 + 2H, · C.H10_to, xt → CH4 + 2H,
C2H6_to, xt → C2H2 + 2H, | b) Etilen ngày nay được dùng làm nguyên liệu quan trọng để sản xuất PE, P.V.C và nhiều hóa chất khác như etanol axetandehit, nên được sản xuất 1 lượng lớn. Câu 6.
- a) CH3-CH2-CH2-CH; _to, xt → CH3-CH=CH-CH; (A) + H2 b) CH3-CH2-CH2-CH;_to, xt → CH2=CH-CH2-CH; (B) + H, c) CH4-CH=CH-CH, – to, xt → CH3–C=C-CH3 (C) + H2 d) CH3-CH=CH-CH; _to, xt → CH2=CH-CH=CH, (D) + H21 e) CH2=CH-CH2-CH; _to, xt → CH2=CH-CH=CH2 (D) + H2 g) CH2=CH-CH2-CH;_to, xt → CH=C-CH2-CH; (E) + H2 CH3-C=C-CH3 + Brz → CH3-CBr=CBr-CH3
– CH2 – CH – CH = CH2 CH2=CH-CH=CH2 + Br2 Br Br
bCH2 – CH = CH – CH2
]
..————-
Br
i
Br
CH3-CH2-C=CH + [Ag(NH3)2]OH → CH3-CH2-C=CAgt
+ H2O + 2NH2 |
Câu 7. | Phản ứng: C,H, + x ) + XCO + HCO
1+x+=x+} = $ = 4
Vậy hiđrocacbon ở thể khí có thể là: CH4; CH4; C3H4; C,H,. Câu 8.
– 3,36 = 0,15 (mol)
+
X
=
X
.
V4114
Ta có: n hỗn hợp A =
22,4
Gọi công thức chung của hai anken là: C H. a) Phản ứng: C H + Br2 → C4H, Bra (mol) 0,15 0,15 Khối lượng bình brom tăng chính là khối lượng của hai anken
M = 3 = 51, 3= 14n = 51,3 = n = 3,66
Vì hai olefin kế tiếp nhau nên CTPT là: CH4 và C4Hg. b) Gọi số mol của C3H6 là a (mol) (M = 42);
và số mol của C4H8 là b (mol) (M= 56) Theo đề bài, ta có hệ phương trình:
la + b = 0,15
142a + 56b = 7,7 Giải hệ phương trình có: a = 0,05; b =0,1.
1
- 2 Cli
| Vậy: %V._ 0, 05 x 100%
Vậy: %VC,H, =
= 33,33%,
.
0,15
%VC.1. = 100% – 33,33% = 66,67% c) Các CTCT có thể có của: | C3H6 là: CH2=CH-CH3 C4Hg là: CH2=CH-CH2-CH2; CH3-CH=CH-CH3;
CH, = C-CH, : . . . . CH,
Câu 9.
2,8 = 0,125 (mol) Ta có: nc,H6 = 22,4
Khi nhiệt phân CH, thu được: C2H4: a (mol); C3Hg: b (mol); Hu: (a + 2b) mol và C2Hg: dư
C2H4 + Br2 → C2H4Br2 (mol) a a
C2H2 + 2Br2 → C_HBr4 (mol) b 26
C2H2 + 2[Ag(NH3)2]OH → AgC = CAg+ + 2H,0 + 4NH3 (mol) b
b
Mà b 2 = 0,005 (mol)
240
Do đó: 28a + 26b = 1,465 x 2 = 2,93 3a = 0,1 (mol)
nh, = a + 2b = 0,1 +0,01 = 0,11 (mol)
>nc,He du = 0,125 – (a + b) = 0,125 – (0,1 + 0,005) = 0,02 (mol)
» Tổng số mol hỗn hợp khí:
0,1 +0,005 + 0,11 +0,02 = 0,235 (mol) Vì là chất khí nên %V = %n
0,1 * 100% Vậy: %V,H, = %nc,H, =
= 42,55%. . 0,235
0,005 x 100% %VC_H, = %nc,H, = “
0,235
= 2,13%;
.
0.11 x 100%
%V1, = %ny, = -0,235
= 46,8%.
% C2H6 = 100% – (42,55% + 2,13% + 46,8%) = 8,52%.
