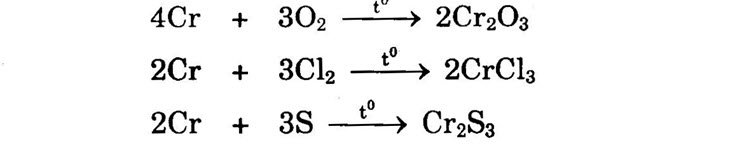| A. KIẾN THỨC CẦN NHỚ
I. Tính chất hóa học 1) Tác dụng với phi kim
2) Tác dụng với nước Crom bền hơn với nước và không khí do có màng oxit rất mỏng, bền bảo vệ. Người ta mạ crom lên sắt để bảo vệ sắt và dùng crom để chế thép không gỉ. 3) Tác dụng với axit Cr + 2HCl → CrCl2 + H2↑ Cr + H2SO4 → CrSO4 + H2↑ Chú ý: – Phản ứng xảy ra khi không có không khí. – Crom không tác dụng với axit HNO3 đặc, nguội và H2SO4 đặc, nguội do bị thụ động hóa. |


Nguồn website giaibai5s.com
- HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 190 Câu 1.
- a) Vị trí của crom trong bảng tuần hoàn: thuộc chu kỳ 4, nhóm VIB. b) Cấu hình electron nguyên tử: 1s2so2p°3so3d4s. c) Khả năng tạo thành các trạng thái oxi hóa khác nhau của crom: do có nhiều electron độc thân ở các obitan 3d và 4s nên trong các hợp chất thì crom có số oxi hóa biến đổi từ +1 đến +6, trong đó số
oxi hóa phổ biến nhất là các số oxi hóa +2, +3, +6. Câu 2. a) Giống nhau:
– Phản ứng với phi kim. – Phản ứng với axit HCl, H2SO4 loãng. – Bên trong không khí và không phản ứng với nước. – Bị thụ động hóa trong axit H2SO4 và HNO3 đặc, nguội.
- b) Khác nhau:
– Nhôm chỉ có 1 trạng thái oxi hóa là +3, còn crom có nhiều trạng thái oxi hóa. Khi phản ứng với axit, nhôm cho hợp chất nhôm (III), còn crom cho hợp chất crom (II).
– Nhôm có tính khử mạnh hơn crom nên nhôm khử được crom (III). Câu 3. a) Chọn B b) Chọn C Câu 4. Phản ứng nhiệt nhôm:
Cr2O3 + 2Al → 2Cr + Al,03 (*) Ta có: nay đàn chó = ,5 (mol).
Từ (*) = nAl = 1,5 (mol) = m1 = 1,5 x 27 = 40,5 (gam). Câu 5. | Lượng crom trong 100 gam hợp kim là:
78
20
= 0,385 (mol).
52
59
Lượng niken trong 100 gam hợp kim là:
0 = 1,356 (mol). Vậy lượng niken ứng với 1 mol crom trong hợp kim là:
= 3,522 (mol). 0,385 –
1,356