| A. KIẾN THỨC CẦN NHỚ
I. Khái niệm, phân loại, danh pháp và đồng phân 1. Khái niệm Khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH4 bằng một hay nhiều gốc hiđrocacbon ta được amin. 2. Phân loại (theo hai cách) a) Theo loại gốc hiđrocacbon: Amin thơm, amin béo, amin dị vòng. b) Theo bậc của amin: Bậc của amin được tính bằng số nguyên tử hiđro trong phân tử amoniac bị thay thế bởi gốc hiđrocacbon (amin . bậc một, bậc hai, bậc ba). 3. Danh pháp – Cách gọi tên theo danh pháp gốc – chức: ank + yl + amin. – Cách gọi tên theo danh pháp thay thế: ankan + vị trí + amin. – Tên thông thường chỉ áp dụng với một số amin. 4. Đồng phân Amin có các loại đồng phân: đồng phân mạch cacbon, vị trí nhóm chức, về bậc của amin. II. Tính chất hóa học 1. Tính chất của chức amin a) Tính bazơ: – Làm quỳ tím hóa xanh:
– Tác dụng với hơi axit HCl tạo “dạng khói trắng”: CH3NH2 + HCl → [CH3NH3]+Cl– metylamin metylamoni clorua – Nhỏ dung dịch HCl vào anilin thì anilin tan dần theo phản ứng: C6H5NH2 + HCl → C6H5NH+3Cl– phenylamoni clorua Anilin không làm đổi màu quỳ tím.
b) Phản ứng với axit nitrợ: – Amin bậc một: tạo ancol hoặc phenol và giải phóng nitơ (ở nhiệt độ thường). C2H5NH2 + HONO → C2H5OH + N2↑ + H2O – Anilin và các amin thơm bậc một: tạo muối điazoni (ở nhiệt độ thấp).
c) Phản ứng ankyl hóa: C2H5NH2 + CH3I → C2H5NHCH3 + HI 2. Phản ứng thế ở nhân thơm của anilin
III. Điều chế 1) Thay thế nguyên tử H của phân tử amoniac
2) Khử hợp chất nitro
|



Nguồn website giaibai5s.com
- HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 61 – 62 Câu 1. Chọn C Câu 2. Chọn C Ta có: m = 3 x 12 = 3,6 (gam); m = 3 x 2 = 0,9 (gam) và m = 3 x 28 = 1,4 (gam)
22,4 | = m = mx – (mg + m + mx) = 5,9 – (3,6 + 0,9 + 1,4) = 0 Vậy X không chứa oxi. | Gọi công thức tổng quát của (X) là: C,H,N. Lập tỉ lệ xỉy t = 38 : 4 = 0,3 : 0,9 : 0,1 = 3 : 9:1
3 công thức của (X) là: C3HgN.
Câu 3.
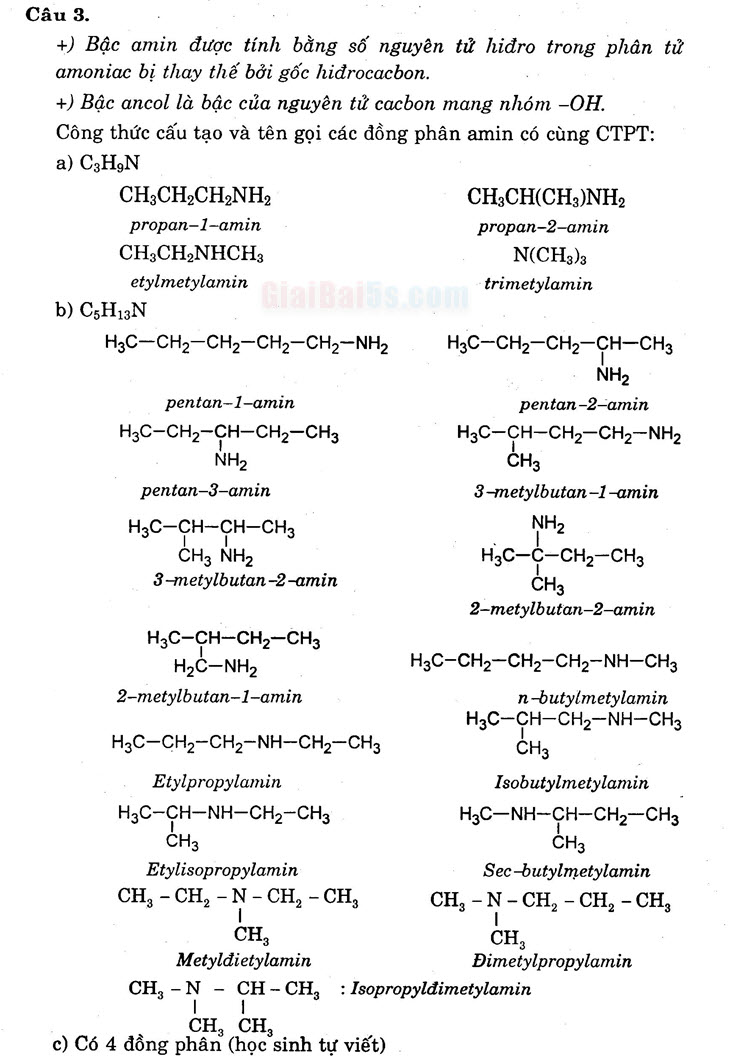
+) Bậc amin được tính bằng số nguyên tử hiđro trong phân tử amoniac bị thay thế bởi gốc hiđrocacbon. +) Bậc ancol là bậc của nguyên tử cacbon mang nhóm –OH. Công thức cấu tạo và tên gọi các đồng phân amin có cùng CTPT: a) C HON CH3CH2CH2NH2
CH2CH(CH3)NH2 propan-1-amin
propan-2-amin CH3CH2NHCH,
N(CH3)2 etylmetylamin
trimetylamin b) C3H13N H3C-CH2-CH2-CH2-CH2-NH2 H3C-CH2-CH2-CH-CH3
. NH2 pentan-1-amin
:: pentan-2-amin H3C-CH2-CH-CH2-CH3 H3C-CH-CH2-CH2-NH2 NH2
CHE pentan-3-amin
3-metylbutan-1-amin H3C-CH-CH-CH3
NH2 CH3 NH2
HzC-¢-CH2-CH3 3-metylbutan-2-amin
CH3
. .” 2-metylbutan-2-amin HzC-CH-CH2-CH3 HAC-NHA
Học-CH2-CH2-CH2-NH-CH3 2-metylbutan-1-amin
n-butylmetylamin
H3C-CH-CH2–NH-CH3 HẠC-CH2-CH2-NH-CH2-CH3
CH3 Etylpropylamin
Isobutylmetylamin H3C-CH-NH-CH2-CH3 | Học-NH-CH-CH2-CH3
CH3
CH3
.
CH
Etylisopropylamin
Sec-butylmetylamin CHI – CH — CH – CHỊ CH – N – CH – CH – CH, CH,
CH, Metyldietylamin
Đimetylpropylamin CH, – N – CH – CHg : Isopropyldimetylamin
CH, CH, c) Có 4 đồng phân (học sinh tự viết)
Câu 4.
- a) Vì các dẫn xuất halogen có cùng số nguyên tử cacbon với các amin sẽ có phân tử khối lớn hơn. b) Lực bazơ: C6H5CH2NH > C6H5NH2 do mật độ electron trên nguyên tử nitơ của C6H5CH3NH2 cao hơn của C6H5NH2, vậy nên C6H5CH2NH2 có thể làm quỳ tím hóa xanh còn C6H5NH2 thì không C6H5CH2NH2 tan vô hạn trong nước do tạo liên kết hiđro với nước | bền hơn C6H5NH2. Câu 5.
- a) Hỗn hợp khí: CH4 và CH3NH2. Sục hỗn hợp khí vào dung dịch HCl: – CH, không phản ứng, thoát ra ngoài, thu được CHệ tinh khiết. – CH3NH2 bị giữ lại do xảy ra phản ứng:
CH3NH2 + HCI → CH3NH3C1 Sau đó, cho NaOH vào để tái tạo CH3NH:
CH3NH2CI + NaOHť → CH3NH2T + NaCl + H2O b) Hỗn hợp lỏng: C6H6, C6H5OH, C6H5NH2. – Cho dung dịch NaOH dư vào và lắc nhẹ: C6H5OH phản ứng và tan vào dung dịch:
| C6H5OH + NaOH -> C6H5ONa (tan) + H2O Chiết để tách dung dịch A chứa C6H5ONa và NaOH ra khỏi chất lỏng B chứa C6H6 và C6H5NH2 (là hai chất không phản ứng với NaOH). – Sục khí CO và A để tái tạo C6H5OH:
C6H50Na + CO2 + H2O → C6H-OH+ NaHCO3 – Cho dung dịch HCl dư vào B: C6H5NH2 phản ứng và tan vào dung dịch còn lại C6H6 nổi lên trên. Chiết lấy C6H6. Sau đó lại cho NaOH
vào phần dung dịch để tái tạo C6H5NH, tương tự như câu (a). .. Câu 6.
- a) C2H5NH2, C6H5NH2, glucozơ, glixerol: – Trích mẩu thử cho mỗi lần thí nghiệm. – Dùng dung dịch AgNO3 nhận ra C2H5NH2: có kết tủa trắng Sau đó tan tạo dung dịch không màu. :
AgNO3 + C2H5NH2 + H2O → Agost + C2H5NH3NO; AgOH + 2C2H5NH2 → (Ag(C2H5NH2)2]OH
– Dùng ngay chính dung dịch AgNOC2H5NH2 mới thu được, nhận ra glucozơ: có kết tủa Ag trắng sáng. – Dùng dung dịch nước brom, nhận ra anilin: có kết tủa trắng.
CoH;NH, + 3Br2 → C6H,Br3NH2+ + 3HBr Còn lại là C2H5NH2. b) CH3NH2, C6H5OH, CH3COOH, CH2CHO: – Dùng quỳ tím nhận ra axit CH3COOH. – Dùng nước brom nhận ra phenol (có 4 trắng) và CH3CHO (mất màu).
– Còn lại là CH3NH2. Câu 7. a) Dùng axit để rửa lọ đựng anilin.
C6H5NH2 + H+ + CH3NH3 b) Dùng giấm khử các amin (tạo ra các hợp chất muối amoni). Câu 8. Phản ứng:
C6H3NH2 + HCl → CH:NH,CI Ta có: none) = 0 = 0,014 (mol)
94 C6H3NH2 + 3Br2 → C&H,BrzNH, + + 3HBr (mol) x + 3x
C&H:OH + 3Br2 → C6H_Br30H + + 3HBr (mol) y → : 3y . y
00 = 0,06 (mol) x + y = 0,02 (**)
> nBrı = 3x + 3y = 3,2 x 300
100 x 160
Từ (*) và (**) 3 nanilin = 0,02 – 0,014 = 0,006 (mol) Vậy: Cact, H = 1 = 0,14M và Cuc.,NH, = 0,08 = 0,06M.
0,1
MIC

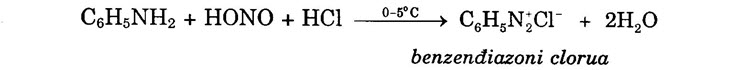
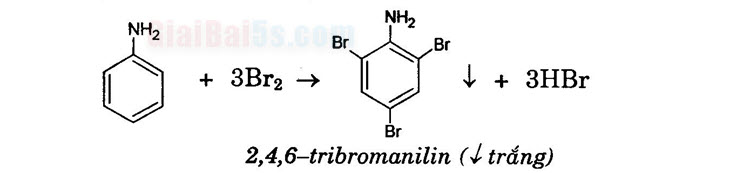 Chú ý: Phản ứng này dùng để nhận biết anilin.
Chú ý: Phản ứng này dùng để nhận biết anilin.