







Nguồn website giaibai5s.com
Câu 1. Hai kim loại nào sau đây có thể điều chế bằng phương pháp nhiệt luyện ? A. Ca và Fe.
- Na và Cu. C. Mg và Zn. D. Fe và Cu. Câu 2. Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O)
được gọi là
- thạch cao nung. B. thạch cao khan. C. đá vôi. D. thạch cao sống. Câu 3. Có thể dùng bình bằng AI để chuyên chở dung dịch nào sau đây ? A. Dung dịch NaOH.
- Dung dịch HCl. C. Dung dịch loãng H2SO4.
- Dung dịch HNO3 đặc nguội. Câu 4. Nhận xét nào sau đây không đúng về vấn đề ô nhiễm môi trường ?
- Các khí CO, CO2, SO2, NO, gây ô nhiễm không khí. B. Nước thải chứa các ion kim loại nặng gây ô nhiễm môi trường nước. C. Nước chứa càng nhiều ion NO, POP thì càng tốt cho thực vật phát triển. D. Hiện tượng rò rỉ dầu từ các dàn khoan, tràn dầu do đắm tàu gây ô nhiễm môi
trường nước biển. Câu 5. Một hỗn hợp bột kim loại X gồm Zn, Fe, Cu, Ag. Để thu được Ag tinh khiết với
khối lượng không đổi, người ta cho hỗn hợp X tác dụng với lượng dư dung dịch A. Fe(NO3)3. B. AgNO3. C. Cu(NO3)
2 D . HNO3 loãng. Câu 6. Oxit nào sau đây không tan trong cả hai dung dịch NaOH loãng và dung dịch HCl
loãng ? A. Cro.
- Feo.
- Fe2O3. D. (r203.
Câu 7. Đun nóng este HCOOCH3 với một lượng vừa đủ dung dịch NaOH, sản phẩm thu
được là A. HCOONa và CH3OH.
- HCOONa và C2H5OH. C. CH3COONa và C2H5OH.
- CH3COONa và CH3OH. Câu 8. Mùi tanh của cá là mùi của hỗn hợp các amin và một số tạp chất khác. Để khử
mùi tanh của cá trước khi nấu nên sử dụng cách nào sau đây ? ” A. Ngâm cá thật lâu trong nước để amin tan đi.
- Rửa cá bằng giấm ăn. C. Rửa cá bằng dung dịch Na2CO3.
- Rửa cá bằng dung dịch thuốc tím để sát trùng. Câu 9. Chất dẻo PE được điều chế từ monome nào sau đây ?
.. . ) tự monome nào sau đây ? A. Etilen.
- Vinyl clorua. C. Etanol. D. Axetilen. ^! . Câu 10. Ở nhiệt độ thường, kim loại Na phản ứng với nước tạo thành
- Na2O và H. B. NaOH và O2. C. Na2O và O2. D. NaOH và H. Câu 11. Trong công nghiệp, để chế tạo ruột phích, người ta thường thực hiện phản ứng | hoá học giữa AgNO3 trong dung dịch NH3 với A. axetilen.
- anđehit fomic. C. saccarozơ. D. glucozơ. Câu 12. Dãy gồm các oxit kim loại đều bị khử bởi Ha khi nung nóng là
g nong la i n A. Al2O3, Fe2O3, ZnO.
- Cr2O3, Bao, CuO. C. Fe3O4, PbO, CuO.
- Cuo, MgO, FeO. Câu 13. Hoà tan 5,6 gam Fe vào dung dịch HNO3 loãng (dư). Sau khi phản ứng kết thúc,
thu được khí NO (sản phẩm khử duy nhất của No) và dung dịch có chứa m gam muối. Giá trị của m là A. 18,0
- 24,2… C. 31,1. D. 11,8. Câu 14. Hoà tan hoàn toàn hỗn hợp X gồm x mol Ba và y mol Al vào nước thu được
V lít khí H2 (đktc) và dung dịch Y. Giá trị của V là A. V = 22,4(x + 3y).
- V = 11,2(2x + 3y). C. V = 22,4(x + y).
- V=11,2(2x + 2y). Câu 15. Thí nghiệm nào sau đây không xảy ra sự hoà tan Cu(OH)2 ?
- Cho Cu(OH)2 vào dung dịch glixerol. B. Cho Cu(OH)2 vào dung dịch propan-1,3-điol. C. Cho Cu(OH)2 vào dung dịch axit axetic. D. Cho Cu(OH)2 vào dung dịch axit fomic.
Câu 16. Triolein không tác dụng với chất (hoặc dung dịch nào sau đây ?
- H2O (xúc tác H2SO4 loãng, đun nóng). B. Cu(OH)2 (ở điều kiện thường).
- Dung dịch NaOH (đun nóng). D. H2 (xúc tác Ni, đun nóng). Câu 17. Đốt cháy hoàn toàn m gam hỗn hợp xenlulozơ, tinh bột, glucozơ, saccarozơ cần
4,48 lít O2 (đktc), thu được 3,51 gam nước. Giá trị của m là A. 5,91.
- 5,81. C. 6,04.
- 5.6. Câu 18. Dung dịch A cho pH > 7 ; dung dịch B cho pH < 7: dung dịch D cho pH = 7.
Trộn A với B thấy xuất hiện bọt khí ; trộn B với D thay xuất hiện kết tủa trắng. A, B, D lần lượt là A. NaOH ; NH4C1; Ba(HCO3)2.
- Na2CO3 : KHSO4 ; Ba NO3)2. C. Na2CO3 ; NaHSO4 ; Ba(OH)2. D. Ba(OH)2 ; H2SO4 : Na2SO4. Câu 19. Cho m gam H2NCH2COOH phản ứng hết với dung dịch KOH dư, thu được
dung dịch chứa 84,75 gam muối. Giá trị của m là A. 66,75.
- 55,65. C. 65,55.
- 50,25. Câu 20. Chất X có công thức phân tử C3H7O2N và làm mất màu dung dịch brom, Tên
gọi của X là A. metyl amino axetat.
- axit a-amino propioni . C. axit B-amino propionic.
- amoni acrylat. Câu 21. Tiến hành bốn thí nghiệm sau :
Thí nghiệm 1: Nhúng thanh Fe vào dung dịch FeCl3. Thí nghiệm 2: Nhúng thanh Fe vào dung dịch CuSO4. Thí nghiệm 3: Nhung thanh Cu vào dung dịch FeCl3. Thí nghiệm 4:Cho thanh Fe tiếp xúc với thanh Cu rồi nhúng vào dung dịch HCl. Trong các thí nghiệm trên, số trường hợp xuất hiện ăn mòn điện hoá là A. 3.
- 4. C.1.
- 2 Câu 22. Đốt cháy m gam P trong O2 dư rối cho P505 sinh ra phản ứng với dung dịch
Ca(OH)2 theo tỉ lệ mol tương ứng là 4 : 10. Cô cạn hỗn hợp sau phan ứng thu được 5,82 gam chất rắn khan. Giá trị gần đúng nhất của m là A. 1,25. B. 1,086. C. 1.28.
- 1.56. Câu 23. Hỗn hợp X gồm các este thuộc loại hợp chất thơm, là đồng phân cấu tạo của
nhau ứng với công thức phân tử C4H8O2. Cho X tác dụng với dung dịch NaOH dư, đun nóng, tổng số muối và tổng số ancol thu được sau phản ứng lần lượt là A. 5 và 2. B. 6 và 1. C. 5 và 1.
- 7 và 2. Câu 24. Cho các nhận định sau :
(1) Protein luôn có khối lượng phân tử lớn hơn cacbohiđrat. (2) Dung dịch các amino axit đều làm đổi màu quỳ tím.
định. (5) Điều chế poli(vinyl ancol) bằng cách trùng hợp ancol vinylic. . .) Trong các nhận định trên, số nhận định sai là A. 1.
- 2. C. 3.
- 4. Câu 25. Cho hỗn hợp bột Al, Fe vào dung dịch chứa Cu(NO3)2 và AgNO, sau khi các
phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn gồm ba kim loại là
- Al, Fe, Ag. B. Fe, Cu, Ag. C. Al, Fe, Cu. D. Al, Cu, Ag? Câu 26. Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 3,26 mol O2, thu được
2,28 mol CO2 và 39,6 gam H2O. Mặt khác, thuỷ phân hoàn toàn a gam X trong dung dịch NaOH, đun nóng, thu được dung dịch chứa b gam muối. Giá trị của b là A. 40,40.
- 31,92. C. 36,72. D. 35,60. Câu 27. Có các nhận xét sau:
(1) Các kim loại Na và Ba đều tan trong nước dư. (2) Độ cứng của Cr lớn hơn độ cứng của Al. (3) Cho K vào dung dịch CuSO4 thu được Cu. (4) Độ dẫn điện của các kim loại giảm dần theo thứ tự Ag, Cu, Al. (5) Có thể điều chế Mg bằng cách cho khí CO khử MgO ở nhiệt độ cao.”
Trong các nhận xét trên, số nhận xét đúng là ! A. 4. B. 3.
. :. D: 2.1 mi! Câu 28. Cho các phát biểu sau:
(1) Saccarozơ được cấu tạo từ hai a-glucozơ. (2) Oxi hoá glucozơ, thu được sobitol. (3) Trong phân tử fructozơ có một nhóm –CHO. (4) Xenlulozơ trinitrat được dùng làm thuốc súng không khói. (5) Trong phân tử xenlulozơ, mỗi gốc glucozơ có ba nhóm -OH. (6) Saccarozơ bị thuỷ phân trong môi trường kiềm. Trong các phát biểu trên, số phát biểu đúng là A. 2.
B.3. C. 5.
- 4. Câu 29. Cho sơ đồ chuyển hoá : Al+X+Y+Z) A1. Các chất X, Y, Z lần lượt là A. Al2O3, AlCl3, Al(OH)3.
- AlCl3, Al(OH)3, Al2O3. C. AIC13, Al(OH)3, NaA102.
H D . Al(OH)3, NaA102, Al2O3. Câu 30. Hỗn hợp X gồm một ancol và một axit cacboxylic đều no, đơn chức, mạch hở,
có cùng số nguyên tử cacbon trong phân tử. Đốt cháy hoàn toàn 51,24 gam X, thu được 101,64 gam CO2. Đun nóng 51,24 gam X với xúc tác H2SO4 đặc, thu được m gam este (hiệu suất phản ứng este hoá bằng 60%). Giá trị của m gần nhất với A. 25,1.
- 28,5. C. 41,8.
- 47,6.
- 5.
Câu 31. Tiến hành các thí nghiệm sau:
(1) Cho Mg vào dung dịch Fe2(SO4)3 dư. (2) Cho dung dịch FeCl2 vào dung dịch AgNO3 dư. (3) Dẫn khí H2 dư qua Fe2O3 nung nóng. (4) Cho Zn vào dung dịch AgNO3. (5) Nung hỗn hợp gồm Al và CuO (không có không khí). (6) Điện phân nóng chảy NaCl với điện cực trơ. Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là A. 3. B. 4. C. 6.
- 5. Câu 32. Axit cacboxylic X tác dụng với amin Y, thu được muối amoni Z có công thức
C3H9O2N. Số công thức cấu tạo của Z phù hợp là A. 2. B. 4. C. 3.
- 1. Câu 33. Hoà tan hoàn toàn 80,7 gam hỗn hợp X gồm Fe(NO3)2 và KCl vào H20 thu
được dung dịch Y. Điện phân Y (có màng ngăn, điện cực trơ) đến khi H2O bắt đầu điện phân ở cả hai điện cực thì dùng điện phân, thu được số mol khí thoát ra ở anot bằng 3 lần số mol khí thoát ra từ catot. Lấy Y cho tác dụng với dung dịch AgNO, dư, thu được y gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của y là A. 86,1.
- 53,85. C. 43,05.
- 29,55. Câu 34. Cho 15,84 gam este no, đơn chức, mạch hở tác dụng vừa đủ với 30 ml dung dịch
MOH 20% (D = 1,2 g/ml) với M là kim loại kiềm. Sau phản ứng hoàn toàn, cô cạn dung dịch thu được chất rắn X. Đốt cháy hoàn toàn X thu được hỗn hợp khí và hơi gồm CO2, H2O và 9,54 gam M CO3. Kim loại M và công thức cấu tạo của este ban đầu là . A. Na và HCOOC2H5.
| B, K và HCOOCH3. C. Na và CH3COOC2H5.
- K và CH3COOCH3. Câu 35. Cho sơ đồ phản ứng sau: X1 + H20
điện phân dung dịch , x + x 1 + H1
có màng ngăn X2 + X4 → BaCO3+ + NaCO3 + H2O X2 + X3 —X, + X5 + H2O X, + X6 + BaSO4 + K2SO, + CO2 + HEO Các chất X, X, X, lần lượt là: A. NaOH, NaCIO, KHSO4.
- KOH, KC103, H2SO4. C. NaHCO3, NaClO, KHSO4.
- NaOH, NaCIO, K SO.
Câu 36. Cho các sơ đồ phản ứng hoá học sau (theo đúng tỉ lệ mol phản ứng): 1
(1) X+2NaOH 1° >Y+ CH3CHO + H20 (2) Y (rắn) + 2NaOH (rắn) + CH4 + 2Na2CO3 Phát biểu nào sau đây đúng? A. X có 8 nguyên tử H trong phân tử. . B. X có khả năng cộng Br, theo tỉ lệ 1:1.
- Trong phân tử X có 2 liên kết T. D. X là hợp chất đa chức. Câu 37. Trong thí nghiệm thử tính tan của khí | hiđro clorua trong nước, nhận xét nào sau
O HCI . . đây không đúng ? A. Có các tia nước màu hồng phun mạnh
vào bình. B. HCl tan tốt trong nước làm giảm áp suất | trong bình. C. Nếu thay khí HCl bằng khí CO2 thì
H2O có pha quỳ tím không có tia nước phun vào bình. D. Nếu thay dung dịch quỳ tím bằng dung dịch phenolphtalein thì không có hiện
tượng gì xảy ra. I . Câu 38. Hỗn hợp E gồm hai este đơn chức, là đồng phân cấu tạo và đều chứa vòng benzen.
Đốt cháy hoàn toàn m gam E cần vừa đủ 8,064 lít khí O2 (đktc), thu được 14,08 gam CO2 và 2,88 gam H2O. Đun nóng m gam E với dung dịch NaOH (dư) thì có tối đa 2,40 gam NaOH phản ứng, thu được dung dịch T chứa 5,32 gam hai muối. Khối lượng muối của axit cacboxylic trong T là
- 1,64 gam. B. 2,72 gam. C. 3,28 gam. D. 2,46 gam. Câu 39. Hoà tan hỗn hợp X gồm Cu và Fe2O3 trong 400 ml dung dịch HCl a mol/l thu
được dung dịch Y và còn lại 1,0 gam Cu không tan. Nhúng thanh Mg vào Y, sau khi phản ứng hoàn toàn nhấc thanh Mg ra thấy khối lượng tăng thêm 4,0 gam và có 1,12 lít khí Ho (đktc) thoát ra (giả thiết toàn bộ lượng kim loại thoát ra đều bám hết vào thanh Mg). Khối lượng Cu trong X và giá trị của a lần lượt là
- 4,2 gam và 0,75. B. 4,2 gam và 1. C. 3,2 gam và 2. D. 3,2 gam và 0,75. Câu 40. X và Y là 2 đồng phân mạch hở có cùng công thức phân tử là C4H9O2N. X tác
dụng với dung dịch NaOH thu được muối X và hợp chất hữu cơ X có phần trăm khối lượng cacbon là 63,16%. Y có trong tự nhiên, khi tác dụng với dung dịch NaOH thu được muối Y có phần trăm khối lượng natri là 18,40%. Cho 5,15 gam hỗn hợp X và Y với tỉ lệ mol nữ : nr = 2 : 3 tác dụng với 100 ml dung dịch KOH 1M thu được dung dịch Z. Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là A. 5,34. B. 5,62. C. 6,54.
- 8,71.
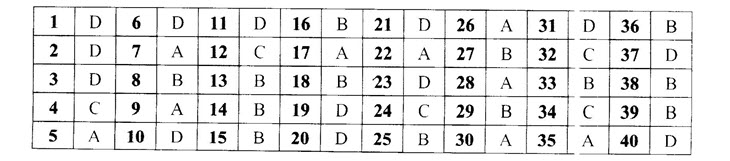
1D6D 11D 16 B 21 D 26 A 31 D 36 B. | 2 | D 7 A 12 ( 17 A 22 A 27 B 32 37 D | 3 D 8 B 13 B 18 B 23 D 28 A 33 B 38 B | 4 0 | 9 | A | 14 B 19 D 24 C 29 B 34C 39 | B
5 A 10 | D 15 B 20 D 25 B 30 A 35 A 40
na
112n+
Câu 30. Hỗn hợp X gồm a mol axit CnH2nO2 và b mol ancol CnH2n-20.
nco, = na + nb = 2.31 (14n = 32).a +(14n + 18).b = 51,24 → 32a + 18b = 18,9 0,590625 < a + b< 1,05 Mà n(a + b) = 2,31 = n = 3; a + b = 0,77 = a = 0.36, b = 0,41.
60
Vậy este là CH5COOC3H7; neste = (0,36. = 0,216 (mol)
100 = m = 116.0.216 = 25,056 (g). Câu 31. Các thí nghiệm thu được kim loại: (2), (3), (4), (5), (6). Câu 32. Z: CHCOONH3CH: HCOONH3CH2CH3 : HC00NH (CH3)2.
:>180a + 74,56 = 80,7
(Fe(NO3)2 : a mol Câu 33. 80,7 gam
numer H2 6
b
BT electron
KCI:b moloncatot
2 + 2a + 2
= b
fa = 0,2 mol 1, Fe2+: 0,1 mol → Ag:0,1 mol
b=0,6 mol 2 CL :0.3 mol – AgCl:0,3 mol > y = mag + magci = 10,8+ 43.05 = 53.85 (gam). Câu 34. 2MOH + M
(mol) X
30.1, 2.20 Mx + 17x = — = 7,2
100 Mx + 30x = 9,54
= Mx = 4,14; x = 0,18 nên M = 23 (Na)
15.84
Meste = 900* = 88 (g/mol) = este là CH3O2
0.18
Từ (1) và (2)= Na và CH3COOC2H5.
Câu 36. (2) Phản ứng với tôi xút;
Tỉ lệ mol 1:24 Y là muối của axit 2 chức : CH2(COONa): (1) = X có 1 chức este với ancol không no, 1 chứa axit.
X là HOOC-CH2-COOCH=CH2.
= X cộng Br, theo tỉ lệ mol 1: 1. Câu 37. Nếu thay dung dịch quỳ tím bằng dung dịch phenolphtalein thì vẫn có các tia
nước phun mạnh vào bình.
Câu 38. Gọi công thức phân tử hai este là C,H,O).
nc(E)=nco, = 0,32 mol; nh(E)= 2n1.0= 0,32 mol Áp dụng ĐL bảo toàn khối lượng :
m=mco, +mh,0-mo, = 0,32.44 +0,16.18 -0,36.32 = 5.44 (gam)
> no(E) = 0,08 mol.
x : y : 2 = nCE : nHỊE : noF)= 0,32 : 0,32 : 0,08 = 8 : 8 : 2 => CTPT của E là C4H8O2.
Thuỷ phân hai este (X, Y) tạo các muối M(1), M(II).
5,44 2,4
” 1:1,58Có một este tác dụng với NaOH theo tỉ lệ mol 1: 2.
ne: n NaOH
136′ 40
X Y
+ 2NaOH → M(I) + M(II) + H2O + NaOH = M(I) + Ancol
136
x + y = 5,44 = 0,04 (x = 0,02 mol 2x + y = 0,06
(y = 0,02 mol 5,44 +0,06.40 – 5,32 -0,02.18 → Mancor =
0 = 108=C6H3 – CH2 -OH.
0,02 Y là HCOOCH2C6H5 ; X là HCOOC6H,CH. = T gồm HCOONa : (x + y) mol và NaO-C6H4-CH3 : x mol. = MHCOONa = (x + y).68 = 0,04.68 = 2,72 (gam)
103
Câu 40. Dựa vào dữ kiện của đề, tìm được công thức cấu tạo của (X): HCOONH3CH2CH=CH2 và (Y): CHỊCH CH(NH2)COOH.
5,15 Ta có, nx +ny = = 0,05 (mol) (nx = 0,02 mol
ny = 0,03 mol inx:ny = 2 : 3
(CH3CH2CH(NH2 )COOK: 0,03 mol Chất rắn khan gồm HCOOK: 0,02 mol
KOH du: 0,05 mol > m=0,03.141 +0,02.84 +0,05.56 = 8,71 (gam).
