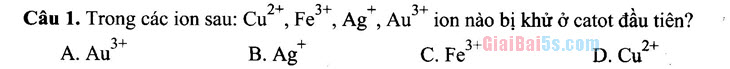








Nguồn website giaibai5s.com
Câu 1. Trong các ion sau: Cu?”, Fe”, Ag, Au* ion nào bị khử ở catot đầu tiên?
- Au + B. Ag C. Fe3+ D. Cu2+
Câu 2. Có thể dùng NaOH rắn để làm khô khí nào sau đây ? A. CO2.
nBa2+ >nso? +Enco3 #sog và CO2 kết tủa hết. =m= 233.n Basoa +153.Bao = 233.0,06+153.0,04 = 20,100(gam)
gam)
.
n
.
Câu 39. nu, = 0,14 mol ; nso, = 0,2625 mol ; ngu sa mol ; M=b mol TH1 : M có hoá trị không đổi
| cu = nso, -CH,=0,1225 mol =mCu = 7,84 gam>M (loại) TH2 :M có hoá trị thay đổi (xét hoá trị 2 và 3)
nm = nu, = 0,14 mol ; 2nCu + 3nm = 2nso, =ncu = 0,0525 mol = mcu = 3,36 gam
mm = 7,84 gam > M= 56 (Fe) Trong 5,6 gam A:nCu = 0,02625 mol ; nFe = 0,07 mol; nAgNO, = 0,17 mol 2nFe + 2ncu> 0,17> 2nFe = Fe tan hết, Cu dư 2nFe + 2nCu tan = 0,17 nCu tan = 0,015 mol + Chất rắn gồm: Ag (0,17 mol); Cu dư :(0,02625 – 0,015 = 0,01125 (mol).
> m=0,17.108 +0,01125.64 = 19,08 (gam) Câu 40. Gọi số mol valin và lysin trong mỗi phần lần lượt là x, y. Phần (1): Val + HCl + Val.HCl; Lys + 2HCl + Lys.2HCl
(mol) х х х у 2у у Phần (2): Val + NaOH + ValNa + H2O (mol) X X
Lys + NaOH → LysNa + H2O (mol) y y
у
(36,5x + 73y = 23,725 (x=0,15 Theo bài ra ta có:22x + 22y = 8,8 ly=0,25
0,15.117 … % mvalin = in 0,15.117+0,25.146.”
sua.100% = 32,47%.
20.15
- SO2
- NH3. D. Cl2.. . Câu 3. Kim loại Al không phản ứng được với chất nào sau đây trong dung dịch loãng ?
- Fe(NO3)3. B. AgNO3. C. NaNO3. D. HNO3. Câu 4. Hiện nay, các hợp chất CFC (cloflocacbon) đang bị hạn chế sử dụng và bị cấm
sản xuất trên phạm vi toàn thế giới vì ngoài gây hiệu ứng nhà kính, chúng còn gây ra hiện tượng A. ô nhiễm môi trường đất.
- ô nhiễm môi trường nước. C. thủng tầng ozon.
| D. mưa axit. Câu 5. Dung dịch nào sau đây không tác dụng với Fe(NO3)2 ? A. HCI
- MgSO4. C. AgNO3 D. Ba(OH)2 Câu 6. Các chất : S, P, C và C2H5OH đều bị bốc cháy khi tiếp xúc với A. CrO3.
- Cr2O3. C. K2Cr2O7. D. Cr2(SO4)3. .. Câu 7. Để có được bơ thực vật từ dầu thực vật ta phải A. hiđro hoá axit béo.
- hiđro hoá lipit lỏng. C. đề hiđro hoá lipit lỏng.
- xà phòng hoá lipit lỏng. Câu 8. Glyxin không phản ứng được với chất nào dưới đây ? A. HCI
- KOH : C. Na2CO3 D. Cu Câu 9. Trùng hợp chất nào sau đây tạo thành tơ olon ? A. CH2=CH2
- CF2=CF2 C. CH2=CHCI
- CH2=CHCN Câu 10. Ở nhiệt độ cao, khí Hy khử được oxit nào sau đây ? A. Fe304
- Cao C. Mgo
- K20 Câu 11. Trong môi trường kiềm, glucozơ tác dụng với chất X tạo ra dung dịch xanh lam.
Chất X là A. NaCl.
- AgNO3. C. Cu(OH)2 D. HNO3. Câu 12. Chất nào sau đây phản ứng với dung dịch NaOH tạo ra kết tủa ?
- Ca(HCO3)2 B. K2CO3 C. Na2CO3 D. CaCl2 Câu 13. Kim loại nào sau đây khử được Fe2+ về Fe? A. Na
- Ba I. C. Cu . D. Mg Câu 14. Cho 0,78 gam kim loại kiềm M tác dụng với nước (dư), thu được 0,01 mol khí H.
Kim loại M là A. Li. B. Na. C. K
- Rb.
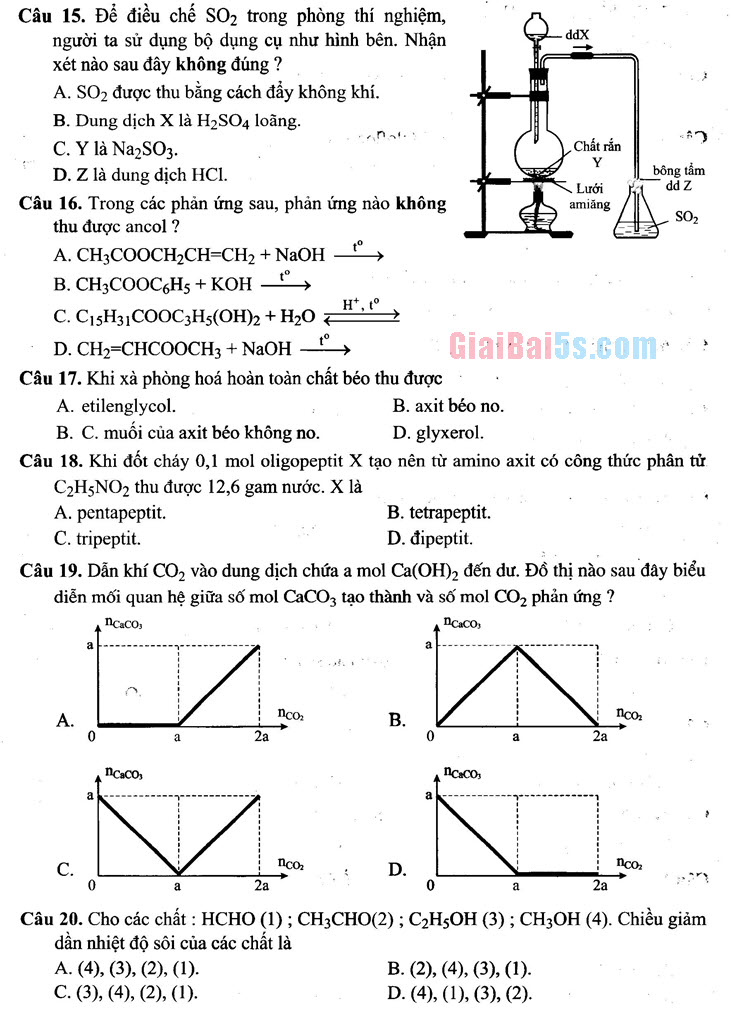
Câu 15. Để điều chế SO2 trong phòng thí nghiệm,
người ta sử dụng bộ dụng cụ như hình bên. Nhận xét nào sau đây không đúng ? A. SO2 được thu bằng cách đây không khí. B. Dung dịch X là H2SO4 loãng. C. Y là Na2SO3.
Chất rắn D. Z là dung dịch HCl. .
|| bông tẩm Lưới
dd z Câu 16. Trong các phản ứng sau, phản ứng nào không
I amiăng thu được ancol ?
_SO2 A. CH3COOCH2CH=CH2 + NaOH → B. CH3COOC6H5 + KOH*
- C13H3 COOC3H5(OH)2 + H20B, · D. CH2=CHCOOCH3 + NaOH Câu 17. Khi xà phòng hoá hoàn toàn chất béo thu được : A. etilenglycol.
. B. axit béo no. . .
. . B. C. muối của axit béo không no. D. glyxerol. Câu 18. Khi đốt cháy 0,1 mol oligopeptit X tạo nên từ amino axit có công thức phân tử
C2H5NO2 thu được 12,6 gam nước. X là A. pentapeptit.
- tetrapeptit. C. tripeptit.
- dipeptit. Câu 19. Dẫn khí CO2 vào dung dịch chứa a mol Ca(OH)2 đến dư. Đồ thị nào sau đây biểu diễn mối quan hệ giữa số mol CaCO, tạo thành và số mol CO2 phản ứng ? Ancaco
nCaCO3
Câu 21. Nung a gam hỗn hợp Al2O3 và Fe3O4 với H2 dư, thu được b gam nước và c gam
chất rắn A. Hoà tan A trong dung dịch HCl dư, thu được 1,008 lít H2 (đktc). Các phản ứng xảy ra hoàn toàn. Giá trị của b là A. 0,18. . B. 0,36. S C . 0,54.
- 1,08. Câu 22. Chất hữu cơ X có công thức phân tử là C3H6O4. Thuỷ phân X bằng dung dịch | NaOH dư, thu được một muối và một ancol. Công thức cấu tạo của X có thể là
- HOOC-CH=CH-OOC-CH3. B. HOOC-COO-CH2-CH=CH2.
- HOOC-CH2-CO0-CH=CH2. D. HOOC-CH2-CH=CH-OOCH. Câu 23. Hàm lượng Ca(H2PO4)2 trong supephotphat kép có độ dinh dưỡng 53,25% là
- 87,75%. B. 70,25%. C. 96,12%. D. 84,45%. Câu 24. Cho các polime :polietilen, poli(vinyl clorua), polistiren, poli(etylen terephtalat),
tơ nitron, tơ capron, tơ visco. Trong các polime trên, số polime có thể được điều chế bằng phản ứng trùng ngưng là A. 2.
B.3.
- C. 4. Câu 25. Thực hiện các thí nghiệm sau ở điều kiện thường:
(a) Cho một ít bột Fe vào dung dịch H2SO4 loãng. (b) Nhỏ vài giọt dung dịch Fe(NO3)2 vào dung dịch AgNO3. (c) Nhỏ vài giọt dung dịch FeCl3 vào dung dịch AgNO3. (d) Cho một ít bột Cr vào dung dịch H2SO4 đặc nguội. Trong các thí nghiệm trên, số thí nghiệm xảy ra phản ứng là A. 1.
- 2. C. 4.
- 3. Câu 26. Đun nóng một lượng chất béo cần vừa đủ 40 kg dung dịch NaOH 15%, giả sử
phản ứng xảy ra hoàn toàn. Khối lượng glixerol thu được là
- 13,8 kg. B.6,975 kg. C. 4,6 kg. D. 8,17 kg. Câu 27. Thực hiện các thí nghiệm sau:
(1) Dung dịch Al(NO3)3 + dung dịch NaOH dư. (2) Dung dịch HCl dư + dung dịch Na2CO3. (3) Al + dung dịch NaOH. (4) Dung dịch NH3 + dung dịch AlCl3. (5) Dung dịch NH4Cl + dung dịch NaOH. (6) Dung dịch Na2CO3 + dung dịch NaHSO4. 5, 4 dung dịch NaHSO4:
..
, , , , , , , , Trong các thí nghiệm trên, số thí nghiệm tạo thành chất khí là A. 3. ..B.5.
C.2.
- 4. Câu 28. Cho các phát biểu sau về khả năng phản ứng của các chất (ở điều kiện thường):
(a) Cu(OH)2 tan được trong dung dịch saccarozơ. . (b) Glucozơ tác dụng với AgNO3 trong dung dịch NH3.
(c) Metyl metacrylat tác dụng với nước brom. (d) Glyxin (H2NCH2COOH) phản ứng được với dung dịch HCl. . Trong các phát biểu trên, số phát biểu đúng là A. 2. B. 4. . C. 1.
- 3. . Câu 29. Nhận xét nào sau đây không đúng ?
- Nhôm là kim loại lưỡng tính, nhôm hiđroxit là bazơ lưỡng tính, nên chúng đều có thể tan trong dung dịch axit và dung dịch kiềm. B. Hỗn hợp 2 kim loại Al và K (với tỉ lệ mol 1 : 1) có thể tan hoàn toàn trong nước. C. Nhôm bền trong không khí là do tạo lớp màng oxit bảo vệ, nhôm bên trong nước do nhôm tác dụng với H2O tạo ra Al(OH)3 ngăn không cho nhôm tiếp xúc với H2O.
- Nhôm có khả năng tan trong các dung dịch NaOH, KHSO4 và HCl. Câu 30. Cho m gam hỗn hợp Y gồm axit axetic, phenol và ancol etylic tác dụng vừa đủ
với Na thu được 19,6 gam hỗn hợp muối X. Đốt cháy hoàn toàn X thu được 10,6 gam muối cacbonat. Nếu cho 30,4 gam Y tác dụng với Na dư, thu được V lít H2 (đktc). Giá trị của V là A. 4,48. B. 5,60. C. 3,36.
- 6,72. Câu 31. Hỗn hợp X gồm Na, Ba và Al. Cho 5 gam X vào nước dư, thu được 2,688 lít khí
H2 (đktc). Mặt khác, cho 5 gam X vào dung dịch NaOH dư, thu được 2,912 lít khí H2 (đktc). Phần trăm khối lượng của Al trong X là A. 36%.
- 54%. . C. 27%. . D. 18%. Câu 32. Có bao nhiêu hợp chất hữu cơ mạch hở có công thức phân tử C3H4O vừa phản
ứng được với H2 (xúc tác Ni, t°), vừa phản ứng được với dung dịch AgNO3 trong NH3 dư, đun nóng ? A. 4 – B. 2 . c.5
- 3 Câu 33. Cho 5,528 gam hỗn hợp X gồm Fe và Cu (nre:nu = 18,6:1) tác dụng với dung
dịch chứa 0,352 mol HNO3, thu được dung dịch Y và khí NO (sản phẩm khử duy nhất của N). Tiến hành điện phân dung dịch Y với điện cực trơ, cường độ dòng điện I=2,4125 A trong thời gian t giây thấy khối lượng catot tăng 0,16 gam (giả thiết kim loại sinh ra bám hết vào catot). Giá trị của t là A. 2920.
- 200. C. 3920.
- 2000. Câu 34. Tiến hành thí nghiệm như hình vẽ bên.
Nhận xét nào sau đây không đúng ? A. Đun nóng CuO trong ống rồi mới dẫn Hạ khí H2 vào. B. Trong thí nghiệm trên, CuO bị khử thành Cu.. C. Sau khi tắt đèn cồn tiếp tục dẫn Họ qua
-H,0 để ống nghiệm nguội hẳn mới đóng khoá dẫn H2. D. Để khử bỏ lớp Cu bám trên bề mặt ống thuỷ tinh, người ta sử dụng dung dịch HNO3.
Câu 35. Tiến hành thí nghiệm với các hoá chất X, Y, Z, T. Hiện tượng được ghi ở bảng sau: Mẫu thử Thí nghiệm
| Hiện tượng x | Tác dụng với Cu(OH)2 trong môi trường kiềm Có màu tím.
Đun nóng với dung dịch NaOH loãng (dư), để Dung dịch xanh Y
nguội. Thêm tiếp vài giọt dung dịch CuSO4. lam.
Đun nóng với dung dịch NaOH loãng (dư). Thêm | Kết tủa Ag trắng, Z
tiếp dung dịch AgNO3 trong NH3, đun nóng. sáng. T | Tác dụng với dung dịch I loãng
Có màu xanh tím. X, Y, Z, T lần lượt là A. lòng trắng trứng, triolein, vinyl axetat, hồ tinh bột. B. triolein, vinyl axetat, hồ tinh bột, lòng trắng trứng. C. lòng trắng trứng, triolein, hồ tinh bột, vinyl axetat.
- vinyl axetat, hồ tinh bột, triolein, lòng trắng trứng. Câu 36. Trong một bình kín chứa 0,7 mol C2H2 ; 1,3 mol H2 và một ít bột Ni. Nung nóng
bình một thời gian, thu được hỗn hợp khí X có tỉ khối so với H2 bằng 8. Sục X vào lượng dư dung dịch AgNO3 trong NH3 đến khi phản ứng hoàn toàn, thu được hỗn hợp khí Y, m gam kết tủa và dung dịch Z. Hỗn hợp khí Y tác dụng vừa đủ với 0,3 mol Br2 trong dung dịch. Khối lượng của Z giảm so với khối lượng dung dịch AgNO3 trong NH3 ban đầu là
- 48,0 gam. B. 96,0 gam. C. 43,2 gam. D. 42,8 gam. Câu 37. Nhỏ từ từ từng giọt cho đến hết 300 ml dung dịch NaHCO, 0,1M; K2CO3 0,2M
vào 100 ml dung dịch HCl 0,2M; NaHSO4 0,6M và khuấy đều thu được dung dịch X. Thêm vào dung dịch X 100 ml dung dịch KOH 0,12M; Ba(NO3)2 1,2M thu được kết tủa Y. Lọc, nung Y đến khi khối lượng không đổi thu được m gam chất rắn. Giá trị của m là A. 22,252.
- 15,300. C. 20,100. D. 21,860. Câu 38. Cho 11,84 gam este (không tham gia phản ứng tráng bạc, có số nguyên tử
cacbon nhỏ hơn 4) phản ứng hoàn toàn với 30 ml dung dịch MOH 20% (D = 1,2 g/ml, với M là kim loại kiềm). Sau khi phản ứng hoàn toàn, cô cạn dung dịch thu được chất rắn X. Đốt cháy hoàn toàn X trong oxi dư thu được 9,54 gam M2CO3 và m gam hỗn hợp gồm CO2, H2O. Giá trị m gần nhất với
- 14,625. B. 14,875. C. 14,445. D. 29,775. Câu 39. Cho 11,2 gam hỗn hợp A gồm Cu và kim loại M (trong đó khối lượng M lớn hơn
khối lượng của Cu) tác dụng hết với HCl dư, thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng (dư), thu được 5,88 lít khí SO2 (đktc, sản phẩm khử duy nhất). Nếu lấy 5,6 gam A tác dụng với 170 ml AgNO3 1M thu được m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn.
m gần nhất với giá trị nào sau đây ? A. 19,05
- 18,35
- 21,35 D. 20,15 Câu 40. Chia m gam hỗn hợp X gồm 2 a-amino axit là valin và lysin thành hai phần bằng
nhau : cho phần một tác dụng hoàn toàn với dung dịch HCl dư, thu được dung dịch Y chứa ( + 23,725) gam muối ; cho phần hai tác dụng hoàn toàn với dung dịch
W
NaOH dư, thu được dung dịch Z chứa (7 + 8,8) gam muối. Phần trăm khối lượng của valin trong hỗn hợp X là A. 67,53%. B. 32,47%. C. 42,81%
57,19%.
1 A 6 A 11 c 16. B 21 D 26 C 31 A 36 D 2 C 7 B 12 A 17 D 22 B 27 D 32C 37 c 3 C 8 D 13 D 18 B 23 A 28 B 33 A 38 A
4 C9 D 14 C 19 B 24 A29 A34C 39 A | 5 | B 10 A 15 D 20 C 25 D 30 A 35 A 40 B] Câu 31. Gọi số mol Na, Ba, Al trong hỗn hợp X lần lượt là x, y, z.
>> 23x + 137y + 272= 5
Cho X + H2O:
Na + H2O-
Na+ + OH
+ -H
Ba + 2H30 —Ba2+ + 2OH + H21 47
min
Al + OH + H2O —
+
= nu, x+y+ (x + 2) = 2x + 4y=0,12
(2)
Cho X + NaOH : nH ==nN. + n
+ án A1 = -x +y+ 2z=
0,13
N
3 + 2H20
. i .
Giải hệ (1), (2), (3)=x-y= 0,02 mol; -mol = %mẠI – $ 100% = 36% Câu 32. Có 5 chất : CH2=CH-CHO, CH3-CH2-CHO, HCOO-CH=CH2, CH=CH-CH2OH,
CH=C-O-CH3. Câu 33. nFe = 0,093 mol ; ngu = 0,005 mol
4HNO3 + 3e + NO + 3NO3 + 2H2O *** (mol) 0,352 0,264 0,264
► 2ncu + 2nfe <0,264 < 2ncu + 3nFe »Dung dịch Y chứa :Cu* (0,005 mol) ; Fe2*(x mol) ; Fe (y mol); NO (0,264 mol). nFe = x + y = 0,093 Áp dụng BT điện tích : 0,005.2 +2x + 3y = 0,264.
. . (2) Giải hệ (1) và (2)= x = 0,025 mol;y= 0,068 mol. nCu bám trên catot = 0,0025 mol. Tại catot: Feb + le + Fe? … .
. Cu2+ + 2e → Cu It ne = = = ne3+ + 2n + = 0,068 + 2.0,025 = 0,073 (mol)=t=2920 giây.
(1)
Câu 37. Nhận thấy nụ <HCO3 +2nco > Ho hết, HCO3 và COỉ dư. “co, (từ HCO3 =x (x+2y=nH+ = 0,08 ={x _[HCO3]_1 =
“co, (từ HCO ) =0,016 [y [COộ 1 2 [“co, (từ CO2 =0,032
SHCOZ (0,014mol); co} (0,028mol); => Dd X
(soź (0,06mol); Nat; kt. nHCO3 >noH- = HCO3 dư và OH hết =Enco3- = 0,028+ 0,012 = 0,04 (mol)
om
