






Nguồn website giaibai5s.com
Câu 1. Kim loại dẫn điện tốt nhất là A. Ag. B. Au. C. Al.
- Cu. Câu 2. Ứng dụng nào sau đây không phải của natri hiđroxit ? A. nấu xà phòng
- chế phẩm nhuộm C. luyện nhôm
- làm thuốc đau dạ dày Câu 3. Kim loại kiềm, kiềm thổ và nhôm có thể được điều chế bằng phương pháp nào
sau đây ? A. điện phân nóng chảy
B, thuỷ luyện C. nhiệt luyện
- điện phân dung dịch Câu 4. Khí nào sau đây gây hiệu ứng nhà kính ? A. O2
- H2 C. N2
- CO2 Câu 5. X là một oxit của sắt. X tác dụng với dung dịch HCl thu được 2 muối. Công thức
phân tử của X là A. FeO.
- Fe2O3. : C. Fe3O4. D. FeO2. Câu 6. Kim loại nào sau đây có nhiều electron độc thân nhất ? A. Cu
- Fe C. Cr
- Ag Câu 7. Công thức nào sau đây không thể là công thức đơn giản của 1 este no, mạch hở ?
- C3H2O2 B. C5H100 C. CsH2O2 D. C4H504 Câu 8. Nhỏ nước brom vào dung dịch chất nào sau đây thấy xuất hiện kết tủa trắng ? A. anilin
- alanin C. đimetylamin D. glyxin Câu 9. Polime nào sau đây được điều chế bằng phản ứng trùng hợp ? A. teflon
- nilon-6,6 C. poli(etylen terephtalat)
- poli(ure-fomandehit) Câu 10. Khí CO không khử được oxit kim loại nào sau đây ? A. CuO B. Fe2O3 C. Mgo
- Fe304 Câu 11. Chất nào sau đây vừa tác dụng với dung dịch HCl vừa tác dụng với dung dịch
NaOH?
- glyxin , B. anilin . C. metylamin D. amoniac Câu 12. Nung thạch cao sống ở 160°C, thu được thạch cao nung. Công thức của thạch
cao nung là A. CaO.
- CaSO4.2H20. C. CaSO4.H20. D. CaSO4. Câu 13. Cho a mol FeS2 và b mol FeCO3 phản ứng với dung dịch HNO3 tạo dung dịch
chứa 1 muối và hỗn hợp khí NO và CO2. Tỉ lệ a : b bằng A. 3:1.
- 1:3. C. 2:1.
- 1:2.
Câu 14. Cho một mẫu nước cứng có chứa a mol Ca, b mol Mg2+ còn lại là ion HCO, .
Số mol Ca(OH)2 cần dùng để làm mất hoàn toàn tính cứng của mẫu nước trên là
- a mol. B. b mol. C. (a + b) mol. D. (a + 2b) mol. Câu 15. Để chứng minh sự ảnh hưởng qua lại của nhóm -OH và vòng benzen trong
phenol (C6H5OH) thì cần cho phenol tác dụng với các chất nào sau đây ? A. Na và nước Br2
- dung dịch NaOH và khí CO2 C. dung dịch NaOH và nước Br2 D. quỳ tím và nước Br2 Câu 16. Khi thuỷ phân những chất nào sau đây chỉ cho glucozơ ? A. saccarozơ, mantozơ, tinh bột
- protein, tinh bột, chất béo C. xenlulozơ, saccarozơ, tinh bột D. tinh bột, xenlulozơ, mantozơ Câu 17. Một loại mùn cưa chứa 60% xenlulozơ được dùng làm nguyên liệu sản xuất
ancol etylic. Nếu dùng 1 tấn mùn cưa trên có thể sản xuất được bao nhiêu lít cồn 70° ? (giả sử hiệu suất của quá trình là 70% ; khối lượng riêng của ancol etylic nguyên chất là 0,8 g/ml)
- 298,125 lít B. 425,926 lít C. 365,675 lít D. 542,734 lít Câu 18. Đốt cháy hoàn toàn một amin đơn chức thì sản phẩm thu được có tỉ lệ mol
nco, :H,O = 8:9. Công thức phân tử của amin là
- C4HųN. B. C4HỌN. C. CzH9N. D. C3H7N. Câu 19. Phản ứng nào sau đây không đúng ?
- MgCO3 to → MgO + CO2 B. Ba(HCO3)2 + NaOH+ BaCO3 + NaHCO3 + H2O C. Na2CO3 + HCl → NaHCO3 + NaCl
- K2CO3 ť→ K20+ CO2. Câu 20. Cho các dung dịch sau lần lượt tác dụng với nhau từng đôi một : NH3,
(CH3)2NH, HCl, C6H5NH3Cl, FeCl3. Số cặp chất xảy ra phản ứng là A. 4.
- 5. C. 6.
- 7. Câu 21. Cho các cặp oxi hoá – khử được sắp xếp theo thứ tự tăng dần (từ trái sang phải)
tính oxi hoá của các ion kim loại : Fe2+/Fe; Cu?* Cu, Fe’ Fe2+, Ag’/Ag. Tiến hành các thí nghiệm sau : (a) Cho sắt vào dung dịch đồng(II) sunfat. (b) Cho đồng vào dung dịch sắt(II) sunfat. (c) Cho bạc vào dung dịch đồng(II) nitrat. (d) Cho bạc nitrat vào dung dịch sắt(II) nitrat. . Trong các thí nghiệm trên, những thí nghiệm có thể xảy ra phản ứng là A. (a) và (c). B. (a) và (d). | C. (b) và (c). D. (b) và (d).
Câu 22. Nhúng quỳ tím vào các dung dịch sau:
(1) H2NCH2CH(NH2)COOH; (2) H2NCH2COONa ; (3) CIH3NCH2COOH; (4) HOOCCH2CH2CH(NH2)COOH; Peter (5) NaOOCCH2CH2CH(NH2)COONa. Những dung dịch làm quỳ tím chuyển sang màu xanh là
- (1), (2), (5). B. (1), (3), (5). C. (2), (3), (5). D. (1), (4), (5). Câu 23. Một loại đá vôi chứa 80% CaCO3 còn lại là tạp chất trơ. Nung m gam đá này
một thời gian thu được 0,78m gam chất rắn. Hiệu suất phân huỷ CaCO3 là A. 78%.
- 50%.
- 62,5%. D. 97,5%. Câu 24. Cho các polime sau : cao su lưu hoá, poli(vinyl clorua), thuỷ tinh hữu cơ,
glicogen, polietilen, amilozơ, nhựa rezol. Số polime có cấu trúc mạch thẳng là A. 6. B.3. C. 4.
- 5. Câu 25. Cho sơ đồ sau:
Fe2O3 +A , Fe +B , FeSO4 +C , FeCl2 +D, Fe(NO3)2A, B, C, D lần lượt là A. AgNO3, CO, BaCl2, CuSO4. B.CO, AgNO3, CuSO4, BaCl2.
- CO, CuSO4, BaCl2, AgNO3. D. CO, CuSO4, AgNO3, BaCl2. Câu 26. Cho các phát biểu sau:
(a) Dùng phản ứng tráng bạc để phân biệt fructozơ và glucozơ. (b) Trong môi trường bazơ, fructozơ chuyển hoá thành glucozơ. (c) Trong dung dịch nước, glucozơ tồn tại chủ yếu ở dạng mạch hở. . . (d) Xenlulozơ và tinh bột là đồng phân của nhau. (e) Saccarozơ có tính chất của ancol đa chức và anđehit đơn chức.
. . Trong các phát biểu trên, số phát biểu đúng là A. 2. B. 1. C. 4.
- 3. Câu 27. Cho hỗn hợp kim loại Mg, Al, Fe vào dung dịch chứa AgNO3, Cu(NO3)2 và
HNO3. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 3 muối và chất rắn Y gồm ba kim loại. Ba muối trong X là A. Mg(NO3)2, Al(NO3)3, Fe(NO3)2. B. Mg(NO3)2, Al(NO3)3, Cu(NO3)2.
- Mg(NO3)2, Fe(NO3)3, AgNO3. 1. D. Mg(NO3)2, Al(NO3)3, Fe(NO3)3. Câu 28. Cho các phát biểu sau :
(a) Thuỷ phân hoàn toàn vinyl axetat bằng NaOH, thu được natri axetat và anđehit fomic. (b) Polietilen được điều chế bằng phản ứng trùng ngưng. (c) Ở điều kiện thường, anilin là chất khí.
(d) Tinh bột thuộc loại polisaccarit. (e) Khi thuỷ phân anbumin của lòng trắng trứng, thu được a-amino axit. (g) Ở điều kiện thích hợp, triolein tham gia phản ứng cộng H2. Trong các phát biểu trên, số phát biểu đúng là A. 3. B. 4.
- 5. . . D. 6. Câu 29. Nung hỗn hợp gồm BaCO3, Fe(OH)3, Al(OH)3, Cu(OH)2 và MgCO3 trong
không khí đến khối lượng không đổi được hỗn hợp chất rắn X. Cho X vào H2O (dư), khuấy đều được dung dịch Y chứa hai chất tan và phần không tan Z. Cho khí CO (dư) đi qua Z nung nóng được hỗn hợp chất rắn E. Biết các phản ứng xảy ra hoàn toàn. Hỗn hợp E gồm A. 1 kim loại và 3 oxit.
- 2 kim loại và 1 oxit. C. 1 kim loại và 2 oxit.
- 2 kim loại và 2 oxit. Câu 30. X là hỗn hợp 2 anđehit đơn chức mạch hở. Cho 0,04 mol X (tương ứng với khối
lượng 1,98 gam) tham gia vào phản ứng tráng bạc, kết thúc phản ứng thu được | 10,8 gam Ag. Mặt khác m gam X tác dụng vừa đủ với 0,35 gam H2. Giá trị của m là A. 9,9.
- 4,95. C. 6,93.
- 5,94. Câu 31. Hỗn hợp X gồm Al và một oxit sắt. Hoà tan hoàn toàn 13,4 gam X trong dung
dịch H2SO4 đặc, nóng (dư), thu được 2,8 lít khí SO2 (sản phẩm khử duy nhất, ở đktc) và dung dịch Y có chứa 41,4 gam muối. Cho dung dịch NaOH dư vào Y, tạo thành m gam kết tủa. Oxit sắt và giá trị của m là A. FeO và 10,70.
- Fe2O3 và 5,35. C. Fe3O4 và 16,05.
- Fe3O4 và 21,25. Câu 32. Trong các chất sau : CH3OH, CH3CHO, C2H5OH, CH3CH2CH2CH2, CH4,
CH3COOC2H5, số chất có thể điều chế được CH3COOH bằng một phản ứng là A. 4.
B.2. C. 3.
- 5. Câu 33. Mắc song song bình (1) chứa dung dịch NaCl với bình (2) chứa dung dịch
AgNO3. Tiến hành điện phân với dòng điện cường độ 19,3 A trong thời gian 25 phút thấy khối lượng catot bình (2) tăng 21,6 gam và ở anot bình (1) chỉ thu được một loại khí X. Thể tích khí X (đktc) đến thời điểm đó là
- 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít. Câu 34. Tiến hành phản ứng nhiệt nhôm hỗn hợp gồm Al và Cr2O3 trong khí quyển trơ
(giả sử chỉ có phản ứng khử oxit kim loại tạo thành kim loại). Sau một thời gian thu được 21,95 gam hỗn hợp X. Chia X thành hai phần bằng nhau. Phần (1) cho phản ứng với dung dịch HCl loãng, nóng (dư), thu được 3,36 lít H2 (đktc). Phấn (2) cho phản ứng với dung dịch NaOH đặc, nóng (dư), thu được 1,68 lít H2 (đktc). Hiệu suất phản ứng nhiệt nhôm là A. 75%.
- 60%. F. C. 25%. D. 40%. Câu 35. Có 4 dung dịch riêng biệt : H2SO4 1M, HNO3 1M, NaOH 1M, HCl 1M. Cho
5 ml mỗi dung dịch vào 4 ống nghiệm và kí hiệu ngẫu nhiên là X, Y, Z, T. Tiến hành thí nghiệm với các dung dịch X, Y, Z, T, kết quả thu được như sau:
– Hai dung dịch X và Y tác dụng được với FeSO4. . . . . . . .” ‘.. – Dung dịch Z có pH thấp nhất trong 4 dung dịch. – Hai dung dịch Y và T phản ứng được với nhau. . Các dung dịch X, Y, Z, T lần lượt là : A. NaOH, HNO3, H2SO4, HCl.
- HCI, NaOH, H2SO4, HNO3. C. HNO3, NaOH, H2SO4, HCI. . D. HNO3, NaOH, HC1, H2SO4. Câu 36. Xà phòng hoá m gam một este đơn chức cần vừa đủ 100 ml dung dịch NaOH 2M.
Cô cạn dung dịch sau phản ứng thu được chất rắn khan Y và hơi hợp chất hữu cơ Z. Khi đốt cháy hoàn toàn Y thu được Na2CO3, H20 và 6,72 lít khí CO2 (đktc). Chất hữu cơ Z bị oxi hoá hết thành anđehit T. T phản ứng với dung dịch AgNO3/NH3 dư thu được Ag theo tỉ lệ nợ nAg = 1: 4. Giá trị của m là A. 17,6.
- 12,0. C. 14,8.
- 14,6. Câu 37. Cho hỗn hợp khí X gồm clo và oxi tác dụng vừa hết với 1,92 gam Mg và 4,48 gam
Fe tạo ra hỗn hợp Y gồm muối clorua và oxit. Hoà tan hoàn toàn Y cần 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào Z thu được 56,69 gam kết tủa. Phần trăm theo thể tích khí Cl2 trong X là A. 51,72%.
- 53,85%. B. 76,70%.. D. 56,36%. Câu 38. Đốt cháy hoàn toàn a mol chất X là este của glixerol với 3 axit cacboxylic đơn
chức thu được b mol CO2 và c mol H2O, biết b− c = 4a. Hiđro hoá hoàn toàn m gam X cần 5,6 lít H2 (đktc) thu được 32 gam Y. Nếu đun m gam X với dung dịch NaOH vừa đủ thì khối lượng muối khan thu được là
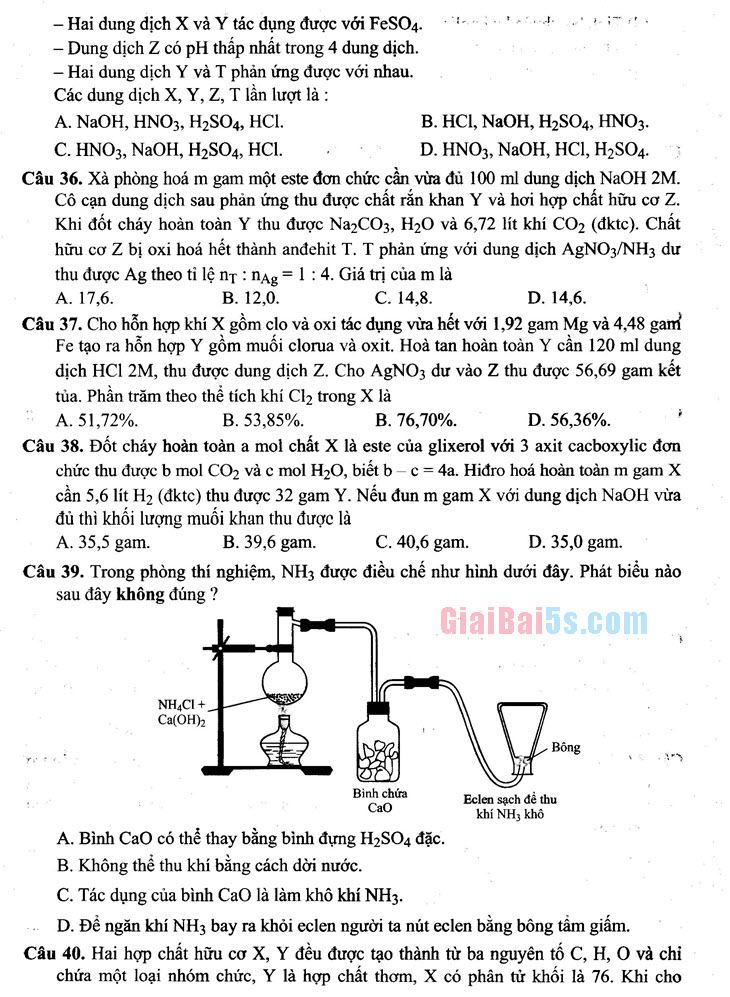
- 35,5 gam. B. 39,6 gam. C. 40,6 gam. D. 35,0 gam. Câu 39. Trong phòng thí nghiệm, NH, được điều chế như hình dưới đây. Phát biểu nào
sau đây không đúng ?
:
:
.
.
.
NH4Cl + H Ca(OH)2
.
|
Bông
.
.
..
Bình chứa
Eclen sạch để thu Cao
khí NH3 khô A. Bình CaO có thể thay bằng bình đựng H2SO4 đặc. B. Không thể thu khí bằng cách dời nước. C. Tác dụng của bình CaO là làm khô khí NH3.
- Để ngăn khí NH3 bay ra khỏi eclen người ta nút eclen bằng bông tẩm giấm. Câu 40. Hai hợp chất hữu cơ X, Y đều được tạo thành từ ba nguyên tố C, H, O và chỉ
chứa một loại nhóm chức, Y là hợp chất thơm, X có phân tử khối là 76. Khi cho
1,14 gam X tác dụng với Na dư, thu được 336 ml khí (đktc). Chất Z (có công thức phân tử trùng với công thức đơn giản nhất) được tạo thành khi cho X tác dụng với Y. Đốt cháy hoàn toàn 1,12 gam Z cần 1,288 lít O2 (đktc), thu được CO2 và H2O có tỉ lệ mol tương ứng là 11 :6. Mặt khác, 4,48 gam X tác dụng vừa đủ với 200 ml dung dịch NaOH 0,2M. Số công thức cấu tạo phù hợp của Z là A. 5.
- 6. C. 9.
- 10.
1 A 6 C 11 A 16 D 21 B 26 B 31 c 36 C 2 D 7 A 12 C 17 B 22 A 27 A 32 D 37 B
3 A 8 A 13 A 18 B 23 C 28 A 33 A 38 D | 4 D 9 A 14 D 19 D 24 D 29 B | 34 A 39 A
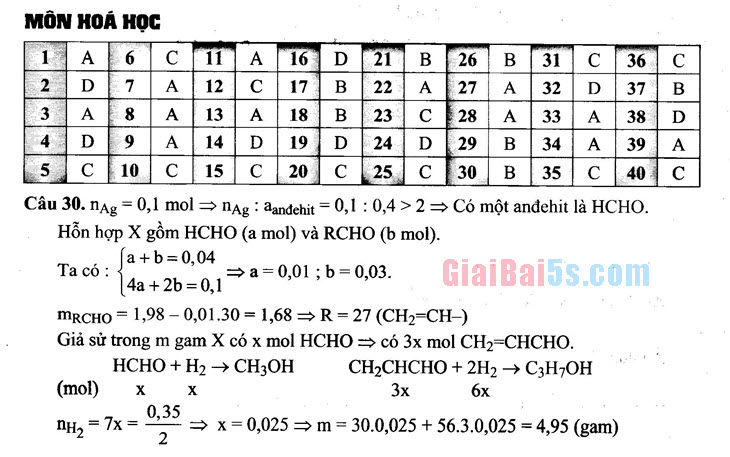
5 C 10 C 15 C 20 C 25 C 30 B 35 C 40 C Câu 30. nAg = 0,1 mol = nAg: aanđehit = 0,1: 0,4 > 24 Có một anđehit là HCHO. | Hỗn hợp X gồm HCHO (a mol) và RCHo (b mol).
a+b=0,04 Ta có : 100 – 14a + 2b = 0,1
> a=0,01 ; b = 0,03. MRCHO = 1,98 -0,01.30 = 1,68 R=27 (CH2=CH-) Giả sử trong m gam X có x mol HCHO» có 3x mol CH2=CHCHO.
HCHO + H2 → CH3OH CH2CHCHO + 2H2 → C3H7OHi (mol) X X
– 3x 6x ny, = 7x = x=0,025 m= 30.0,025 + 56.3.0,025 = 4,95 (gam)
:
3HZOH
Câu 31. Gọi x, y, z là số mol Al, Fe và O trong X.
27x + 56y +162 = 13,4 (x=0,0667 {3x + 3y – 2z=0,125.2={y=0,15 =
=-(Fe304)
(z=0,2
(342. – +400. Y = 41,4
=>m=mFe(OH), = 0,15.107 = 16,05(gam)
Câu 32. Các chất : CH3OH, CH3CHO, C2H5OH, CH3CH2CH2CH3, CH3COOC2H5 có
thể điều chế được CH3COOH bằng một phản ứng.
It
19,3.25.60
Câu 33. ne
F* 96500
=0,3 (mol)
.
.
0,05 0,1
ME
Bình 1: Ag + le > Ag Bình 2: 2Cl + Cl2 + 2e (mol)
0,2 0,2 V = 0,05.22,4 = 1,12 (lít) Câu 34. 2Al + Cr203 1°, A1203 + 2C1 (Al:a mol
(P2:3a =0,075.2=a=0,05 21,95
Cr:b mol <=10,975 gam
P1:3a + 2b =0,15.23b=0,075 Al2O3 :c mol
=c=0,0375= d=0,0125 Cr2O3:d mol BT(NT+KL)
Al:0,125 mol
0.05 -0.0125 (Cr2O3: 0,05 mol
0,05
BTelectron
0,05-0,0125 100%= 75%
H=
;
975
Câu 36.
((Y)RCOONa+O3 → Na2CO3 +CO2 +H20 (X)RCOOR’ + NaOH →
|(Z)R’OH_[0] >(T)R “CHO_+AgNO3/NH3>ntinAg =1:4 Este X đơn chức ở Anđehit T đơn chức 4T là HCHO=z là CH3OH
NRCOOR’ = NRCOONa = NNaOH = 0,2 mol
Áp dụng BTNT Na: nNa,CO, = nNaOH = 0,1 mol.
–
=
2
Áp dụng BTNT C: số nguyên tử C trong Y = “Na2CO3 *”CO2 = 0,1+0,
DRCOONa
0,2 =Y là CH3COOH 9X là CH3COOCH3> m = 0,2.74 = 14,8 (gam)
Câu 37. nFe = NMg =0,08 mol, nuci = 0,24 mol. vigen
Mg_+Cl2,02 y_+0,24 mol HCI, daz_+AgNO3, Mg2+, Fe3+ 4: (Fe
AgCl, Ag nư = 0,24 mol ; n (trong Y) = nH+ = 0,12 mol >no, =0,06 mol Gọi số mol Clạ trong X là x mol, số mol Ag trong kết tủa là y mol. MesMg2+ 4200
O + 2e → 0-2(trongY) ?
0,12 0,08 (mol)
0,24 Fe – > Fe3+ + 3e
2C1(C12) + 2e – →2014 (mol) 0,08
0,24
1 X 2x
Ag+ + le — + Ag
(mol) y y Áp dụng bảo toàn electron = 2x +y= 0,16. – Mặt khác : nAgCl =nc = 2nCl, +nHCl = 2x+ 0,24 (mol). .
#mkết tủa = 143,5(2x + 0,24) + 100y = 56,69 (gam)
x=0,07 mol; y=0,02 mol %Vci, = 53,85%. Câu 40, nx = 0,015 mol ; nH2 = 0,015 mol 8X có 2 nhóm –OH, Mx = 768x: CgH6(OH)2. –
no, = 0,0575 mol; nco, = 11a mol; nh,0= 6a mol. Áp dụng ĐLBTKL: 1,12 + 0,0575.32 = 113.44 + 6a.183a = 0,005. →nco, = 0,055 mol ; nh,0=0,03 mol = no(z) = 0,025 mol.
nc(z): NH(Z): No(z) = 0,055 : 0,03.2: 0,025 = 11 : 12:5=Z:CjH1205 nz= 0,02 mol ; nNaOH = 0,04 mol X là ancol (có 2 nguyên tử oxi), Y là axit (số oxi chẵn);Z có 5 nguyên tử oxi (lẻ), tác dụng NaOH tỉ lệ mol 1:23Z có 1 nhóm este, 1 nhóm ancol và 1 nhóm COOH. X (C3H6(OH)2)+Y+Z (CH2O5) + H2O=Y là C4H6O. Y : HOOC-C6H4-COOH (0, m, p có 3 công thức cấu tạo ; X có 2 công thức cấu tạo
3 Số công thức cấu tạo của Z là 9
