| I. TÓM TẮT LÝ THUYẾT
1. Tính chất vật lý: chất khí, nhẹ nhất trong các chất khí tan rất ít trong nước. 2. Tính chất hóa học: – Tác dụng với oxit kim loại: (có tính khử mạnh)
3. Ứng dụng: – Làm nhiên liệu, sản xuất amoniac, axit… – Làm chất khử để điều chế kim loại từ oxit của chúng. – Dùng để bơm vào kinh khí cầu… |
II. GIẢI BÀI TẬP SGK.
Bài 1. Viết phương trình hóa học của các phản ứng hiđro khử các oxit sau:
a. Sắt (III) oxit; b. Thuỷ ngân (II) oxit; C. Chì (II) oxit.
HƯỚNG DẪN GIẢI
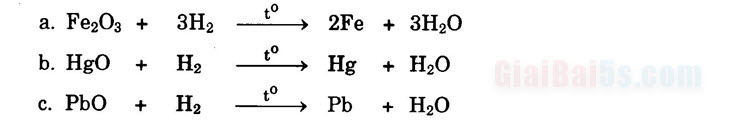
Bài 2. Hãy kể những ứng dụng của hiđro mà em biết?
HƯỚNG DẪN GIẢI
Ứng dụng của hiđro: sản xuất axit, amoniac, chất khử oxit kim loại.
Bài 3. Chọn cụm từ thích hợp trong khung để điền vào chỗ trống trong các câu sau:
| tính oxi hóa; tính khử; chiếm oxi; nhường oxi; nhẹ nhất |
– Trong các chất khí, hidro là khí… ….. Khí hiđro có…
– Trong phản ứng giữa H2 và CuO, H2 có …………… vì……….. của chất khác; CuO
có…………. vì …………. cho chất khác.
HƯỚNG DẪN GIẢI
– Trong các chất khí, hiđro là khí nhẹ nhất. Khí hidro có tính khử.
– Trong phản ứng giữa H2 và CuO, H2 có tính khử vì chiếm oxi của chất khác; CuO có tính oxi hóa vì nhường oxi cho chất khác.
Bài 4. Khử 48 gam đồng (II) oxit bằng khí hiđro. Hãy:
a. Tính số gam đồng kim loại thu được;
b. Tính thể tích khí hidro (đktc) cần dùng.
HƯỚNG DẪN GIẢI
 Bài 5. Khử 21,7 gam thuỷ ngân (II) oxit bằng hiđro. Hãy:
Bài 5. Khử 21,7 gam thuỷ ngân (II) oxit bằng hiđro. Hãy:
ạ. Tính số gam thủy ngân thu được;
b. Tính số mol và thể tích khí hiđro (đktc) cần dùng.
HƯỚNG DẪN GIẢI
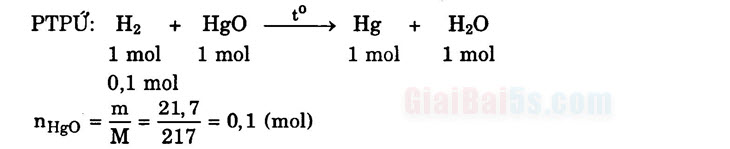
a. nHg = 0,1 mol → mHg = 0,1.201 = 20,1 (g)
b. nH2 = 0,1 mol → VH2 = 0,1.22,4 = 2,24 (l)
Bài 6*. Tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc).
HƯỚNG DẪN GIẢI
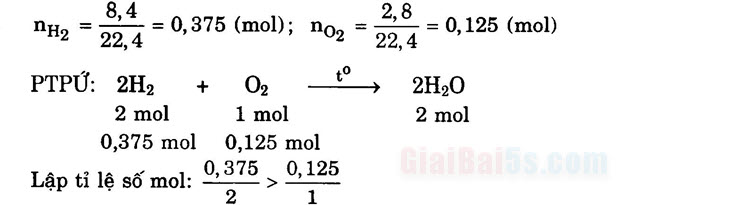 Vậy H2 dư, O2 hết
Vậy H2 dư, O2 hết
nH2O = 0,125.2 = 0,25 (mol)
mH2O = 0,25.18 = 4,5 (g).
Nguồn website giaibai5s.com
