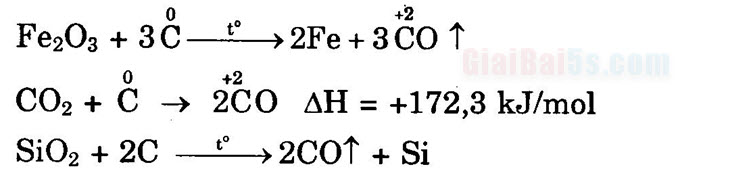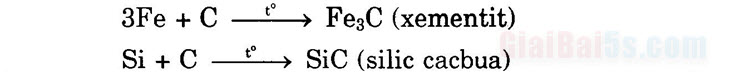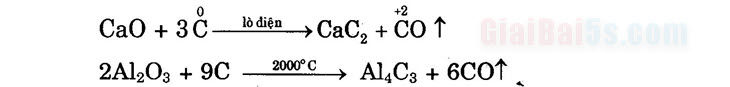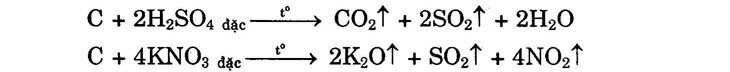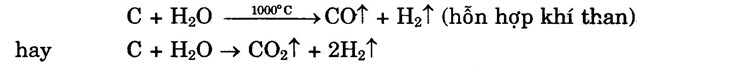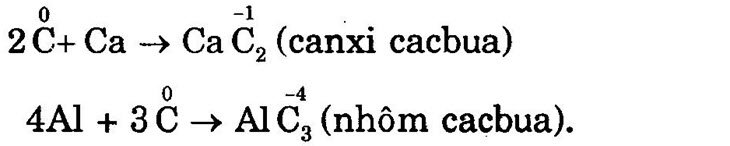| A. KIẾN THỨC CẦN NHỚ
1. Tính khử a) Tác dụng với oxi: b) Tác dụng với hợp chất: +) Tác dụng với oxit: +) Nếu dư cacbon, sẽ tạo cacbua:
Đặc biệt với CaO và Al2O3 thì:
+) Tác dụng với chất oxi hóa:
+) Ở nhiệt độ cao, cacbon tác dụng với hơi H2O:
2. Tính oxi hóa b) Tác dụng với kim loại: |
B. HƯỚNG DẪN GIẢI VÀ ĐÁP ÁN BÀI TẬP SGK TRANG 82


Nguồn website giaibai5s.com
Câu 1.
- a) Các dạng thù hình của cacbon:
– Kim cương – Than chì – Than vô định hình (than gỗ, than xương, than cốc).
– Kim cương và than chì có tính chất vật lí khác nhau là vì: +) Kim cương có cấu trúc tứ diện, đều đặn. +) Than chì có cấu trúc lớp, các lớp liên kết yếu với nhau.
- b) Kim cương và than chì là hai dạng thù hình của nguyên tố cacbon vì khi nung nóng có không khí, kim cương và than chì đều phản ứng với oxi, tạo thành khí cacbon đioxit:
C + O2 + + CO2 Câu 2.
- a) Hầu hết các hợp chất của cacbon là hợp chất cộng hóa trị vì cacbon là phi kim yếu, khả năng nhường và nhận electron đều yếu. Trong các hợp chất cacbon thường có khả năng tạo thành cặp electron chung.
- b) Tính chất hóa học đặc trưng của cacbon: +) Tính khử:
- Tác dụng với oxi: C+0, $co,
- Tác dụng với hợp chất: 8+ PbO, Pb + cỏ, Chú ý: Cacbon khỉ được nhiều oxit kim loại trừ oxit của kim loại từ
Al trở về đầu dãy hoạt động hóa học của kim loại. +) Tính oxi hóa:
- Tác dụng với hiđro: C + 2H2 – Ni,500°C+ CHỊ
- Tác dụng với kim loại: 2C + Ca tỳ CaC, Câu 3. Đáp án: C. Câu 4. Cân bằng: Cr + CO2(k) + 2COR)
Ban đầu: 0,2 1 0 Cân bằng: 1- a da
| (a: số mol CO, tham gia phản ứng).
Vì cân bằng trong hệ dị thể chỉ chú ý đến nồng độ mol chất khí. Do đó:
[ 2a 1 [Colý | 22, 4] _ a 002 – )
(2a) 0,002(1 – a) K = [co] » 1-a
(22,4) 22,4 22,4 = 4a? + 0,0448a – 0,0448 = 0. Giải phương trình ta được: giá trị phù hợp là: a = 0,1 Vậy ở trạng thái cân bằng: nco = 2,0 x 0,1 = 0,2 (mol), nco, = 1,0 – 0,1 = 0,9 (mol) và n = 0,2 – 0,1= 0,1 (mol)