| A. KIẾN THỨC CẦN NHỚ
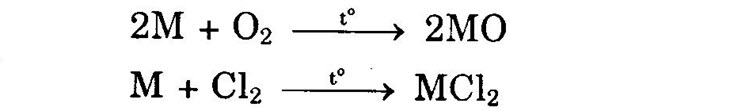
I. Tính chất hóa học 1. Tác dụng với phi kim → tạo oxit bazơ hoặc muối.
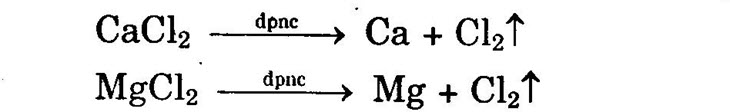
2. Tác dụng với axit M+2H+ → M2+ + H2↑ 3. Tác dụng với nước M + 2H2O → M(OH)2 + H2↑ (M là Ca, Ba, Sr) Chú ý: Be không tác dụng với HọO dù ở nhiệt độ cao. II. Điều chế Điện phân muối halogenua nóng chảy của chúng.
|


Nguồn website giaibai5s.com
- b) Năng lượng ion hóa giảm vì số lớp electron tăng, số electron ngoài cùng đều là 2 electron nên lực hút giữa hạt nhân và electron ngoài cùng giảm, do đó năng lượng cần để tách electron ra khỏi nguyên tử giảm. c) Thế điện cực chuẩn E,-, giảm vì tính oxi hóa của các ion kim loại giảm, tính khử của các kim loại tăng.
- d) Tính khử tăng vì E., giảm. Câu 4.
- a) Ba2+/Ba; Sr2+/Sr; Ca2+/Ca; Mg2+/Mg; Be2+/Be. b) He: 1s22s. Mg: 18-2s22p@3s. c) Bạn đọc tự vẽ đồ thị và rút ra nhận xét. d) Kim loại kiềm thổ có số oxi hóa +2 là do nguyên tử dễ dàng tách
hai electron trong các phản ứng hóa học. Câu 5.
– Năng lượng ion hóa ảnh hưởng tới tính khử của nguyên tử kim loại kiềm thổ. – Năng lượng ion hóa của kim loại kiềm thổ nhỏ nên tính khử mạnh. – Thế điện cực chuẩn E N ảnh hưởng tới tính khử của kim loại kiềm thổ. EM của kim loại kiềm thổ có giá trị nhỏ nên kim loại
kiềm thổ có tính khử mạnh. Câu 6. Chọn B Câu 7. Ta có: n = pV. 1 x 6,11 : 1H, – RT – 0,082 x (273+25) –
= 0,25 (mol) : | Phản ứng: R + 2H2O + R(OH)2 + H21 (mol) 0,25 : +0,25
= Mg = 1 = 40: canxi (Ca).
MS
:
.
.
R 0,25
10
R